登录/
注册
登录/
注册
西洛他唑
Xiluotazuo
Cilostazol

本品为6-[4-(1-环己基-1H-四氮唑-5-基)丁氧基]-3,4-二氢-2-(1H)-喹诺酮。按干燥品计算,含C20H27N5O2应为98.0%~102.0%。
本品为白色或类白色结晶性粉末;无臭。
本品在冰醋酸或三氯甲烷中易溶,在N,N-二甲基甲酰胺中溶解,在甲醇或无水乙醇中微溶,在水、0.1mol/L盐酸溶液或0.1mol/L氢氧化钠溶液中几乎不溶。
熔点 本品的熔点(通则0612)为157~161℃。
①本品能改善由于慢性动脉闭塞症引起的慢性溃疡,肢体疼痛、发冷及间歇性跛行等缺血性症状。辅助治疗由动脉粥样硬化、血栓闭塞性脉管炎、糖尿病所致肢体缺血症及大动脉炎。②预防脑梗死复发。③近年来文献报道,本品与阿司匹林、氯吡格雷合用(三联抗血小板治疗)在急性冠状动脉综合征或高危患者支架植入后可改善治疗后血小板活性亢进并减少主要心血管事件的发生率(尚需进一步研究证实),本品也可用于冠状动脉支架植入术后不能耐受阿司匹林或氯吡格雷时的替代治疗。
口服 成人 一次50~100 mg,一日2次,可根据年龄及病情适当增减剂量。
(1)药效学 本品通过抑制血小板及血管平滑肌内环磷酸腺苷-磷酸二酯酶(cAMP-PDE)活性,从而增加血小板及平滑肌内cAMP浓度、发挥抗血小板聚集及扩张血管作用。抑制 ADP、肾上腺素、胶原及花生四烯酸诱导的血小板第一相、第二相聚集和释放反应,呈剂量相关性。服药后3~6小时血小板聚集被明显抑制。口服100mg对血小板体外聚集的抑制较相应量阿司匹林强7~78倍(阿司匹林对血小板第一相聚集无效)。本品不干扰血管内皮细胞合成血管保护性前列环素(PGI2),对慢性动脉闭塞患者,采用体积描记法显示本品能增加足、腓肠肌部位的组织血流量,使下肢血压指数上升、皮肤血流增加及四肢皮温升高,并改善间歇性跛行。
(2)药动学 本品在肠道内吸收,血浆蛋白结合率在95%以上,主要分布于胃、肝脏、肾脏,中枢神经系统分布很少。成人一次口服100mg,2~4小时血药浓度达到峰值,几天后达到稳态。广泛在肝脏经细胞色素P450酶(主要为CYP3A4,少数为CYP2C19)代谢,产生两个活性代谢产物。主要经尿、少部分经粪便排泄,消除半衰期为11~13小时。
主要为血管扩张引起的头痛及心悸等,个别患者血压轻度升高;其次为消化系统症状,如腹胀、恶心、呕吐、腹痛等;少数患者服药后肝功能异常,尿素氮、肌酐及尿酸升高,皮疹、瘙痒。其他偶有白细胞减少、皮下出血、周围水肿、消化道出血、鼻出血、血尿、眼底出血等报道。
(1)对本品过敏者禁用。
(2)出血性疾病患者(血友病、毛细血管脆性增加性疾病、活动性消化性溃疡、血尿、咯血、功能失调性子宫出血等或有其他出血倾向者)禁用。
(3)各种严重慢性心力衰竭患者禁用。
(4)哺乳期妇女或计划/可能妊娠的妇女禁用。
(5)美国FDA妊娠期用药安全性分级为C。
(1)前列腺素E能与本品起协同作用,增加细胞内cAMP,从而增强疗效。
(2)本品与CYP3A4抑制药(如地尔硫草、酮康唑、伊曲康唑、红霉素)或CYP2C19抑制药(如奥美拉唑)合用,可引起血药浓度升高、不良反应增加,故剂量需减少。
西洛他唑胶囊:50 mg。
西洛他唑片:(1)50 mg;(2)100 mg。
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集754图)一致。
有关物质照高效液相色谱法(通则0512)测定。
溶剂 乙腈-水(25∶75)。
供试品溶液 取本品约25mg,置100ml量瓶中,加乙腈25ml,超声使溶解,用水稀释至刻度,摇匀。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用溶剂稀释至刻度,摇匀,精密量取5ml,置50ml量瓶中,用溶剂稀释至刻度,摇匀。
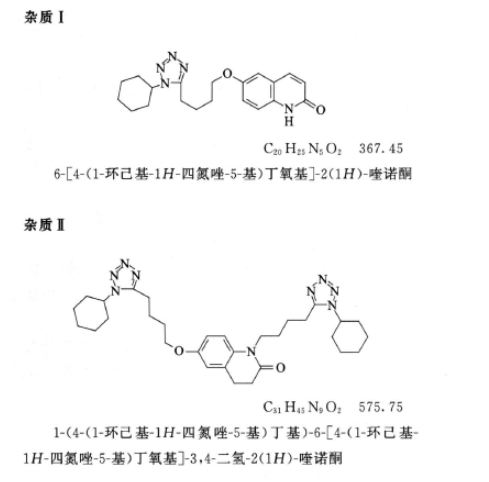
系统适用性溶液 取西洛他唑和杂质 I 对照品各约10mg,置200ml量瓶中,加乙腈50ml超声溶解后,用水稀释至刻度,摇匀。
灵敏度溶液 精密量取对照溶液5ml,置25ml量瓶中,用溶剂稀释至刻度,摇匀。
色谱条件 用辛基硅烷键合硅胶为填充剂(Kromasil 100-5 C8柱,4.6mmX150mm,5μm或效能相当的色谱柱);以水为流动相A,乙腈为流动相B,按下表进行梯度洗脱;柱温为40℃;流速为每分钟1.0ml;检测波长为254nm;进样体积20μl。

系统适用性要求 系统适用性溶液色谱图中,调节色谱条件,使主成分色谱峰的保留时间约为15分钟;出峰顺序依次为杂质 I 与西洛他唑,两峰之间的分离度应大于3.0。灵敏度溶液色谱图中,主成分峰高的信噪比应大于10。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,杂质 I 和杂质 Ⅱ(相对主峰保留时间约为1.4)的峰面积乘以校正因子(均为1.7)不得大于对照溶液主峰面积(0.1%);其他单个杂质峰面积不得大于对照溶液主峰面积(0.1%),校正后各杂质峰面积的和不得大于对照溶液主峰面积的4倍(0.4%),小于灵敏度溶液主峰面积的峰忽略不计。
残留溶剂 照残留溶剂测定法(通则0861第二法)测定。
供试品溶液 取本品,精密称定,加N,N-二甲基甲酰胺溶解并定量稀释制成每1ml中约含75mg的溶液,精密量取4ml,置20ml顶空瓶中,再加水6.0ml,摇匀,立即密封。
对照品溶液 分别取甲苯、二氯甲烷、丙酮与乙醇,精密称定,加N,N-二甲基甲酰胺定量稀释制成每1ml中分别约含66.8μg、45μg、375μg与375μg的混合溶液,精密量取4ml,置20ml顶空瓶中,再加水6.0ml,摇匀,立即密封。
色谱条件 以5%苯基-95%甲基聚硅氧烷(或极性相近)为固定液的石英毛细管柱为色谱柱;起始温度为35℃,维持7分钟,以每分钟25℃的速率升温至220℃,维持5分钟;进样口温度为130℃;检测器温度为250℃;顶空瓶平衡温度为80℃,平衡时间为60分钟。
系统适用性要求 对照品溶液色谱图中,各成分峰之间的分离度均应符合要求,理论板数按乙醇峰计算不低于7000。
测定法 取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度 按外标法以峰面积计算,甲苯、二氯甲烷、丙酮与乙醇的残留量均应符合规定。
氯化物 取本品0.50g,加水50ml,置水浴上加热10分钟,并不时振摇,放冷,滤过,取续滤液25ml,依法检查(通则0801),与标准氯化钠溶液4.5ml制成的对照液比较,不得更浓(0.018%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品约25mg,精密称定,置100ml量瓶中,加乙腈适量超声使溶解,用乙腈稀释至刻度,摇匀,精密量取2ml,置10ml量瓶中,用流动相稀释至刻度,摇匀。
对照品溶液 取西洛他唑对照品,精密称定,加乙腈溶解并用流动相定量稀释制成每1ml中约含50μg的溶液。
系统适用性溶液 见有关物质项下。
色谱条件 用辛基硅烷键合硅胶为填充剂;以水-乙腈(60∶40)为流动相;检测波长为254nm;进样体积20μl。
系统适用性要求 系统适用性溶液色谱图中,出峰顺序依次为杂质I与西洛他唑,两峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
抗血小板聚集药。
密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
