登录/
注册
登录/
注册
加巴喷丁
Jiabapending
Gabapentin
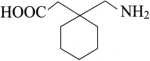
C9H17NO2 171.24
本品为1-(氨甲基)环己基乙酸。按干燥品计算,含C9H17NO2应不得少于98.5%。
本品为白色或类白色结晶或结晶性粉末;无臭。
本品在水中易溶,在乙醇中微溶,在三氯甲烷中不溶。
12岁以上,伴或不伴继发性全面发作的部分性发作癫痫患者。常与其他抗癫痫药物合用。
口服 (1) 成人 第1日300mg,第2日600mg,分2次服;第3日900mg,分3次服。以后根据临床情况可继续增加至维持量,维持量900~1800mg。但剂量增至一日2400~3600 mg亦能耐受。
(2)老年人使用剂量由肾功能肌酐清除率决定。调节方案为:①肌酐清除率>60 ml/min者,一日最大剂量<1200mg(一次400mg,一日3次);②30~60 ml/min者,一日最大剂量<600 mg(一次300 mg,一日2次);③15~30 ml/min者,一日最大剂量<300
mg(一次300 mg.一日1次);④<15 ml/min者,一日最大剂量<150 mg(一次300 mg,隔日1次)。
【儿科用法与用量】12岁以下的剂量未定。12~18岁的剂量与成人同。
(1)药效学 加巴喷丁为人工合成的γ-氨基丁酸(GABA)类似物,抗癫痫作用机制尚不清楚。它对GABA受体无激动作用,也不抑制GABA的再摄取与降解,它能与L型钙通道蛋白结合,但不影响钙内流。有报道本品可能促进GABA的释放。
(2)药动学 口服吸收快,达峰时间(tmax)为2~3小时。吸收过程可饱和,口服300mg时,生物利用度(F)约65%;口服600mg时约42%;口服1600mg时约35%。在体内分布广,可通过血-脑屏障,脑脊液中药物浓度约为血浓度的20%,脑组织内药物浓度可达血浓度的80%;可从乳汁分泌。血浆蛋白结合率很低(<5%),正常肾功能状态下,表观分布容积(Vd)为0.9L/kg。在体内不被代谢,以原形药物从尿中排出,其排泄率与肌酐清除率成正比。半衰期(t1/2)为5~7小时;肾功能异常者t1/2延长达13小时,但在透析中可在3.8小时清除。有效治疗浓度不肯定,一般有效浓度>2μg/ml(11.7μmol/L)。在口服苯妥英钠同时口服400mg每日3次后浓度为2~4.8μg/ml(11.7~28μmol/L)。
(1)较常见的有共济失调,站立不稳;头晕、嗜睡、眼球震颤;外周性水肿。较少见的不良反应有遗忘、疲劳、抑郁、易激动、心境不稳、敌对行为及其他情绪和精神方面改变。罕见粒细胞减少症,一般没有症状。偶有发热、咳嗽、下背痛及排尿困难等。
(2)过量的症状为严重腹泻、复视、严重的头昏、嗜睡和严重构音障碍,口齿不清,最严重者致死。
(3)严重的反应有Stevens-Johnson综合征(罕见)、癫痫发作、昏迷。
(1)对本品过敏者。
(2)美国FDA妊娠期药物安全性分级为口服给药C.
(1)用药之前应当注意对本品是否过敏。
(2)哺乳期妇女用药对乳儿的危害不能排除。
(3)肾功能减退和老年患者应注意减少药物剂量,减量标准应与肌酐清除率成比例。
(4)抗酸药能减少本品的吸收20%以上,因此必须在服制酸剂2小时后服用。
(5)本品口服后可出现假性蛋白尿和白细胞减少。
(6)使用本品,自杀的风险增加。
(1)饮酒或与中枢抑制药合用使中枢抑制作用增强。
(2)与含铝、镁的抗酸药合用可减少吸收。
加巴喷丁胶囊:(1)100 mg;(2)300 mg;(3)400 mg。
加巴喷丁片:300 mg。
(1)取本品约2mg,加水2ml使溶解,加茚三酮约2mg,加热,溶液显蓝紫色。
(2)本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。
酸碱度 取本品0.50g,加水10ml溶解后,依法测定(通则0631),pH值应为6.5~8.0。
溶液的澄清度与颜色取本品0.50g,加水10ml溶解后,溶液应澄清无色;如显色,与黄绿色1号标准比色液(通则0901第一法)比较,不得更深。
氯化物 取本品0.25g,依法检查(通则0801),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.020%)。
氰化物 取本品1.0g,依法检查(通则0806第一法),应符合规定。
有关物质照高效液相色谱法(通则0512)测定。
溶剂取磷酸二氢钾1.2g,加水1000ml溶解,用5mol/L氢氧化钾溶液调节pH值至6.9。
供试品溶液 取本品适量,精密称定,加溶剂溶解并定量稀释制成每1ml中约含14mg的溶液。
对照溶液取杂质Ⅰ对照品约14mg,精密称定,置10ml量瓶中,加溶剂5ml,振摇使溶解,精密加入供试品溶液1ml,用溶剂稀释至刻度,摇匀,精密量取1ml,置100ml量瓶中,用溶剂稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取磷酸二氢钾1.2g,加水940ml溶解,用5mol/L氢氧化钾溶液调节pH值至6.9)-乙腈(94:6)为流动相A,以磷酸盐缓冲液(取磷酸二氢钾1.2g,加水700ml溶解,用5mol/L氢氧化钾溶液调节pH值至6.9)-乙腈(7:3)为流动相B,按下表线性梯度洗脱;流速为每分钟1.5ml;柱温为40℃;检测波长为210nm;进样体积20μl。
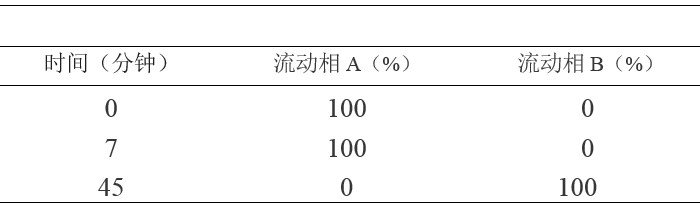
系统适用性要求对照溶液色谱图中,出峰顺序依次为加巴喷丁、杂质Ⅰ,两峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度供试品溶液色谱图中如有与对照溶液中杂质Ⅰ峰保留时间一致的色谱峰,按外标法以峰面积计算,不得过0.1%,其他单个杂质峰面积不得大于对照溶液中加巴喷丁峰面积(0.1%),其他各杂质峰面积的和不得大于对照溶液中加巴喷丁峰面积的5倍(0.5%),小于对照溶液中加巴喷丁峰面积0.3倍的色谱峰忽略不计。
残留溶剂照残留溶剂测定法(通则0861第二法)测定。
供试品溶液 取本品约0.2g,精密称定,置顶空瓶中,精密加水5ml使溶解,密封。
对照品溶液取甲醇、二氯甲烷、甲苯与吡啶各适量,精密称定,加水溶解并定量稀释制成每1ml中分别约含0.12mg、24μg、35.6μg与8μg的混合溶液,精密量取5ml置顶空瓶中,密封。
色谱条件 用5%二苯基-95%二甲基聚硅氧烷(或极性相近)为固定液的毛细管柱为色谱柱;起始温度为40℃,维持5分钟,再以每分钟10℃的速率升温至240℃;进样口温度为100℃,不分流进样,检测器温度为260℃;顶空瓶平衡温度为85℃,平衡时间为30分钟。
系统适用性要求对照品溶液色谱图中,各峰之间的分离度均应符合要求。
测定法 取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度按外标法以峰面积计算甲醇、二氯甲烷、甲苯与吡啶的残留量均应符合规定。
干燥失重 取本品,以五氧化二磷为干燥剂,常温减压干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取本品1.0g,依法检查(通则0821第一法),含重金属不得过百万分之二十。
取本品0.15g,精密称定,加冰醋酸20ml,振摇使溶解后,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显蓝绿色,并将滴定结果用空白试验校正,即得。每1ml高氯酸滴定液(0.1mol/L)相当于17.12mg的C9H17NO2。
抗癫痫药。
密封保存。
杂质Ⅰ
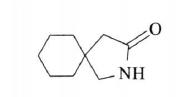
C9H15NO 153.22
2-氮杂螺[4.5]癸烷-3-酮
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
