登录/
注册
登录/
注册
磷酸咯萘啶
LinsuanLuonaiding
MalaridinePhosphate
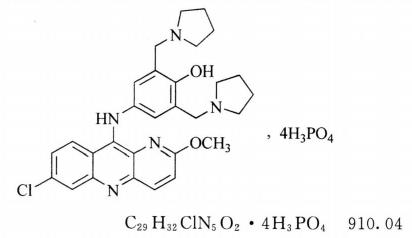
本品为10-[[3',5'二(吡咯烷-1-基甲基)-4'-羟基苯基]氨基]-2-甲氧基-7-氯苯并[b]-1,5-萘啶四磷酸盐。按干燥品计算,含C29H32ClN5O2·4H3PO4应为98.0%~102.0%。
本品为黄色至橙黄色结晶性粉末;无臭,具引湿性。
本品在水中溶解,在乙醇或乙醚中几乎不溶。
用于治疗各种疟疾,特别是耐氯喹虫株所致的恶性疟。
成人①口服第1日服2次,一次0.3g,间隔6小时,第2、3日各服1次,一次0.3g。②肌内注射首次160mg,间隔6小时和24小时各给80mg。③静脉滴注把肌内注射每次用量加入5%葡萄糖注射液250~500ml中,于2~3小时滴完。24小时总剂量320mg。
【儿科用法与用量】口服一日总剂量24mg/kg,分3次服。
【儿科注意事项】(1)严重心、肝、肾脏病患者慎用。
(2)用药后尿呈红色。
(1)药效学 本品为苯并萘啶的衍生物,对间日疟和恶性疟原虫的裂殖体均有杀灭作用。咯萘啶对伯氏疟原虫红内期超微结构的影响首先见于复合膜肿胀,呈多层螺纹膜变;食物泡融合,色素凝集,这些变化呈进行性加重;随后影响线粒体、内质网,核糖体致密,染色质凝集。药物作用4小时后,已见滋养体结构瓦解。裂殖体受影响稍迟,亦出现线粒体肿胀及色素凝集。咯萘啶与氯喹的相同作用点是食物泡,而前者还有第2个作用点即复合膜。可能通过破坏复合膜的结构与功能以及食物泡的代谢活力而起迅速杀虫作用。
(2)药动学 口服与肌内注射后,分别约于1.5小时和0.75小时血药浓度达高峰。肌内注射生物利用度(F)>90%,口服则约为40%。半衰期(t1/2)为2~3日。吸收后以肝内含量最高。从尿中排泄1%~2%。
口服后部分患者出现胃部不适、稀便,偶有恶心、呕吐、头昏、头痛等,偶见窦性心动过缓、心律不齐,偶见皮疹。反应均轻微,停药后即消失。肌内及静脉给药均未见不良反应。
对本药过敏者禁用。
(1)严重心、肝、肾脏病患者慎用。
(2)严禁静脉注射。
(3)肌内注射后局部有硬块,每次注射应改变部位。
(4)用药后尿呈红色。
(5)孕期及哺乳期用药尚不明确。
(1)与磺胺邻二甲氧嘧啶、乙胺嘧啶合用有增效作用,可减少再燃及防止、延缓耐药性的产生。
(2)与伯氨喹合用,有较好的根治间日疟作用。
磷酸咯萘啶肠溶片:0.1g。
磷酸咯萘啶注射液;2ml:80mg。
(1)取有关物质项下供试品溶液,作为供试品溶液;另取磷酸咯萘啶对照品适量,加流动相A溶解并稀释制成每1ml中约含0.2mg的溶液,作为对照品溶液。照有关物质项下的方法,取供试品溶液与对照品溶液各20/1,分别注入液相色谱仪,记录色谱图;供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取本品,加磷酸盐缓冲液(pH7.0)溶解并稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在260nm与276nm的波长处有最大吸收。
(3)取本品80mg,加水10ml使溶解,移至分液漏斗中,加二氯甲烷10ml与氨试液1ml,振摇2分钟,静置分层,取二氯甲烷层用无水硫酸钠过滤,室温下挥干滤液,取残渣以五氧化二磷为干燥剂,减压干燥2小时,照红外分光光度法(通则0402)测定。本品红外光吸收图谱应与同法处理的磷酸咯萘啶对照品的图谱一致。
(4)取本品约20mg,加水5ml溶解后,加氨试液使沉淀完全,滤过,滤液显磷酸盐的鉴别反应(通则0301)。
酸度 取本品1.0g,加水25ml溶解后,依法测定(通则0631),pH值应大于2.4。
氯化物 取本品0.10g,加水4ml使溶解,加20%碳酸钠溶液5ml,摇匀,使沉淀完全,用5号垂熔玻璃漏斗滤过,容器用水15ml分次洗涤、滤过,合并滤液,加水使成25ml,依法检查(通则0801),与标准氯化钠溶液3.0ml制成的对照液比较,不得更浓(0.03%)。
水中不溶物 取本品2.0g,加水25ml振摇使溶解,放置30分钟,用105℃恒重的4号垂熔玻璃堆堪滤过,沉淀用水15ml分次洗涤,在105℃干燥4小时,遗留残渣不得过4mg(供注射用)或7mg(供口服用)。
有关物质照高效液相色谱法(通则0512)测定。临用新制。
供试品溶液 取本品适量,加流动相A溶解并稀释制成每1ml中约含0.2mg的溶液。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相A稀释至刻度,摇匀。
系统适用性溶液 取磷酸咯萘啶适量,加水溶解并稀释制成每1ml中约含0.2mg的溶液,置100℃水浴加热2小时,放冷,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(SepaxsapphireC18,4.6mm×250mm,5μm,孔径100A或效能相当的色谱柱);以磷酸盐缓冲液(取磷酸二氢钾6.81g,加水1000ml溶解,加三乙胺1ml,用磷酸调节pH值至2.8)-甲醇(85∶15)为流动相A,甲醇为流动相B,按下表进行梯度洗脱;检测波长为278nm;进样体积20μl。
时间(分钟)流动相A(%)流动相B(%)
0 100 0
5 100 0
35 50 50
45 50 50
55 100 0
60 100 0
系统适用性 要求系统适用性溶液色谱图中,调节流速使磷酸咯萘啶主峰的保留时间约为21分钟,相对保留时间约为1.1处的杂质峰与咯祭嚏峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(1.0%),各杂质峰面积的和不得大于对照溶液主峰面积的2倍(2.0%)。
甲醛 取本品50.0mg,加水2ml使溶解,加5%碳酸钠溶液4ml,搅匀,滤过,滤液加硫酸溶液(1→2)3ml,冷却后加品红亚硫酸试液5ml,在20~30℃保温120分钟,如显色,与新制的甲醛溶液(每1ml中含甲醛10海的水溶液)1.0ml用同一方法制成的对照液自上向下比较,不得更深(0.02%)。
四氢吡咯 取本品10μg,加水2ml溶解后,加5%碳酸钠溶液2ml,搅拌,滤过,滤液加新制的亚硝基铁氰化钠乙醛试液1ml,摇匀,5分钟内不得显蓝紫色。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过4.0%(通则0831)。
取本品约0.2g,精密称定,加冰醋酸40ml,加热振摇使溶解,放冷,照电位滴定法(通则0701),用高氯酸滴定液(0.1mol/L)滴定。每1ml高氯酸滴定液(0.1mol/L)相当于30.33mg的C29H32ClN5O2·4H3PO4。
抗疟药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
