登录/
注册
登录/
注册
替莫唑胺
Timozuoon
Temozolomide
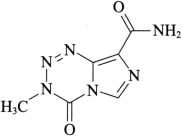
C6H6N6O2 194.15
本品为3,4-二氢-3-甲基-4-氧代咪唑并[5,1-d]1,2,3,5-四嗪-8-甲酰胺。按干燥品计算,含C6H6N6O2应为98.0%~102.0%。
本品为白色至微红色粉末;无臭。
本品在二甲基亚砜中略溶,在水中微溶,在甲醇中极微溶解,在乙醇中几乎不溶,在冰醋酸中微溶。
胶质瘤,胶质母细胞瘤,星形细胞瘤。
口服本药每一疗程28天,最初剂量为按体表面积一次150mg/m²,一日1次,在28天为一治疗周期内连续服用5天。
(1)药效学 本品为咪唑并四嗪类具有抗肿瘤活性的烷化剂。在体循环生理pH状态下,迅速转化为活性产物MTIC(3-甲基-(三嗪-1-)咪唑-4-甲酰胺)。MTIC的细胞毒作用主要表现为DNA分子上鸟嘌呤第6位氧原子上的烷基化以及第7位氮原子的烷基化。通过甲基化加成物的错配修复,发挥细胞毒作用。
(2)药动学 临床前数据提示本品能迅速通过血-脑屏障,进入脑脊液。成年患者口服本品后,被迅速吸收,最早在服药后20分钟就可达到血药峰浓度(平均时间为0.5~1.5小时)。血浆清除率、分布容积和半衰期都与剂量无关。本品的蛋白结合率低(10%~20%),因此估计不会与蛋白结合率高的药物发生相互作用。口服14C-本品后7天内粪便内排泄的14C为0.8%,表明药物是完全吸收的。口服后,24小时尿内的原形药占剂量的5%~10%左右,其余是以AIC(4-氨基-5-咪唑-盐酸羧酰胺)形式或其他极性代谢物排泄到尿中。
本品药代动力学的群体分析表明本品血浆清除率与年龄、肾功能或吸烟无关。
儿科患者的AUC比成人患者高,但是儿童和成人每周期的最大耐受剂量(MTD)都是1000mg/m²。
(1)主要的不良反应包括恶心、呕吐、倦怠和血液学反应。恶心、呕吐、头痛和倦怠的发生频率最高。这些不良反应通常为NCI通用毒性标准(NCIcommontoxicityeriteria,CTC)1或2级(轻至中度),且为自限性,用止吐药即可控制恶心和呕吐。重度恶心和呕吐(CTC3或4级)的发病率分别为10%和6%。
(2)骨髓抑制(血小板减少症和中性粒细胞减少症)为剂量限制性不良反应。通常在治疗的第1个周期发生,不累积。
(1)对本品及辅料过敏者禁用。
(2)由于替莫唑胺与达卡巴嗪均代谢为MTIC,对达卡巴嗪过敏者禁用。
(3)对本药或达卡巴嗪过敏、严重骨髓抑制的患者、妊娠期妇女禁用。
(1)对于接受42~49天合并治疗者需要预防卡氏肺囊虫性肺炎发生。严重肝功能异常或肾功能异常者慎用。本药不应用于哺乳期妇女。
(2)对重度肝肾功能不全的患者和70岁以上患者给药时,应谨慎。
(3)不得咀嚼和打开胶囊。如果无意间打开或破坏了胶囊,须对胶囊内容物万分小心,避免吸入或与皮肤、黏膜接触。应避免让儿童和宠物接近本品。
(1)服用雷尼替丁不改变替莫唑胺及MTIC的C及AUC;
(2)服用丙戊酸可使替莫唑胺清除率降低5%;
替莫唑胺胶囊:(1)5mg;(2)20mg;(3)50mg;(4)100mg。
(1)取本品,加冰醋酸溶液(5→1000)溶解并定量稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在254nm与330nm的波长处有最大吸收,在240nm与279nm的波长处有最小吸收。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集1216图)一致。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,加流动相溶解并稀释制成每1ml中含1.0mg的溶液。
对照品溶液 取杂质Ⅰ对照品适量,加流动相溶解并稀释制成每1ml中含1.0mg的溶液。
对照溶液 精密量取供试品溶液与对照品溶液各1ml,置同一200ml量瓶中,用流动相稀释至刻度,摇匀。
色谱条件用十八烷基硅烷键合硅胶为填充剂;以甲醇-0.5%醋酸溶液(10:90)为流动相;检测波长为254nm;进样体积20μl。
系统适用性 要求对照溶液色谱图中,出峰顺序依次为:杂质Ⅰ与替莫唑胺。理论板数按替莫唑胺峰计算不低于9000,替莫唑胺峰与相邻杂质峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至替莫唑胺峰保留时间的2.5倍。
限度 供试品溶液色谱图中如有杂质Ⅰ峰,其峰面积不得大于对照溶液替莫唑胺峰面积(0.5%);其他单个杂质峰面积不得大于对照溶液替莫唑胺峰面积(0.5%);各杂质峰面积的和不得大于对照溶液替莫唑胺峰面积的2倍(1.0%)。
二甲基亚砜照残留溶剂测定法(通则0861第三法)测定。
内标溶液 取N-甲基吡咯烷酮适量,加N,N-二甲基甲酰胺制成每1ml中约含1mg的溶液。
供试品溶液 取本品0.25g,精密称定,置10ml量瓶中,精密加入内标溶液1ml,用N,N-二甲基甲酰胺稀释至刻度,摇匀。
对照品溶液 取二甲基亚砜25mg,精密称定,置100ml量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,精密量取5ml,置10ml量瓶中,精密加内标溶液1ml,用N,N-二甲基甲酰胺稀释至刻度,摇匀。
色谱条件 以聚乙二醇为固定液;柱温为200℃;检测器温度为240℃;进样体积1μl。
测定法 精密量取供试品溶液与对照品溶液,分别注入气相色谱仪,记录色谱图。
限度 按内标法以峰面积计算,应符合规定。
干燥失重 取本品1.0g,以五氧化二磷为干燥剂,在60℃减压干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加流动相溶解并定量稀释成每1ml中约含替莫唑胺0.1mg的溶液。
对照品溶液 取替莫唑胺对照品,精密称定,加流动相溶解并定量稀释成每1ml中约含替莫唑胺0.1mg的溶液。
色谱条件 见有关物质项下。
系统适用性 要求理论板数按替莫唑胺峰计算不低于9000,替莫唑胺峰与相邻杂质峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
抗肿瘤药。
遮光,密封,在冷处保存。
杂质 Ⅰ
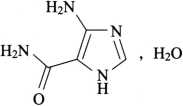
C4H6N4O・H2O 144.13
4-氨基-5-氨基甲酰基咪唑一水合物
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
