登录/
注册
登录/
注册
甲氨蝶呤
Jia’anDieling
Methotrexate
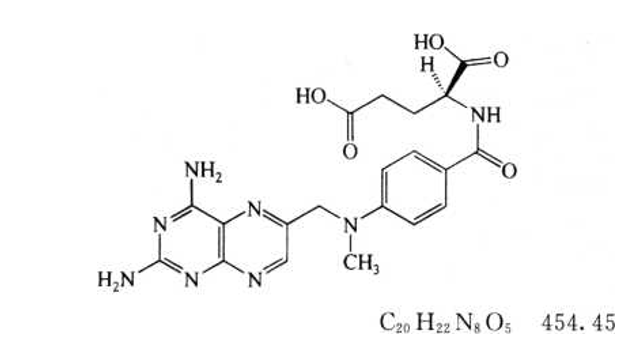
本品为4-氨基-10-甲基叶酸及结构相似物的混合物,主要成分为L-(+)-N-[4-[[(2,4-二氨基-6-蝶啶基)甲基]甲氨基]苯甲酰基]谷氨酸。按无水物计算,含C20H22N8O5应为98.0%~102.0%。
本品为橙黄色结晶性粉末。
本品在水、乙醇、三氯甲烷或乙醚中几乎不溶;在稀碱溶液中易溶,在稀盐酸中溶解。
比旋度 取本品,精密称定,加0.05mol/L碳酸钠溶液溶解并定量稀释制成每1ml中约含10mg的溶液,用2dm的测定管依法测定(通则0621),比旋度为+19°至+24°。
用于各类型急性白血病,特别是急性淋巴细胞白血病、恶性葡萄胎、绒毛膜上皮癌、乳腺癌、恶性淋巴瘤特别是非霍奇金恶性淋巴瘤和蕈样肉芽肿、头颈部癌、卵巢癌、宫颈癌、睾丸癌、支气管肺癌、多发性骨髓瘤和各种软组织肉瘤,高剂量用于骨肉瘤。鞘内注射可用于预防和治疗脑膜白血病以及恶性淋巴瘤的神经系统侵犯。本品对银屑病也有一定疗效。
(1)口服①成人一次10~15mg,一周1~2次;蕈样肉芽肿患者可一日2.5~5mg,连服数周甚或数月。
(2)肌内注射或静脉注射①成人一次15~50mg,一周1~2次。②甲氨蝶呤大剂量疗法:按体表面积一次1~5g/m²,溶于氯化钠注射液或葡萄糖氯化钠注射液中于4~6小时滴完。自用药前1日开始至用药后1~2日每天补液3000ml,并用碳酸氢钠碱化尿液,每日尿量应不少于2000ml。开始用药后24小时起每3小时肌内注射亚叶酸钙9~12mg,连用3~6次或直至甲氨蝶呤血药浓度降至5×10-8mol/L以下。
(3)鞘内注射一次10~15mg,每3~7日1次,注射速度宜缓慢,注入溶液量不能超过抽出脑脊液量。
(4)腔内注射一次30~40mg,一周1次,抽出胸腔积液量少于500ml时酌减。
(5)联合化疗CMF(环磷酰胺、甲氨蝶呤和氟尿嘧啶),主要用于乳腺癌;CMC(环己亚硝脲、甲氨蝶呤和环磷酰胺),主要用于支气管肺癌;COMP(环磷酰胺、长春新碱、甲氨蝶呤和泼尼松)以及CAMP(环磷酰胺、多柔比星、甲氨蝶呤和泼尼松或丙卡巴肼),主要用于恶性淋巴瘤等。
【儿科用法与用量】口服、肌内注射、静脉注射诱导每日3.3mg/m²,维持15~20mg/m²,每周2次。
静脉注射白血病时可达1~5g/m²,实体瘤8~12g/m²,每3周1次,需用四氢叶酸钙解救。
鞘内注射根据不同年龄一次可用8~15mg。
【儿科注意事项】(1)骨髓抑制、肝肾功能损害及胃肠道反应。
(2)大剂量应用可引起高尿酸血症肾病,长期用药可引起咳嗽、气短、肺炎或肺纤维化。
(1)药效学 由于四氮叶酸是在体内合成嘌呤核苷酸和嘧啶脱氧核苷酸的重要辅酶,本品作为一种叶酸还原酶抑制药,主要抑制二氢叶酸还原酶而使二氢叶酸不能被还原成具有生理活性的四氢叶酸,从而使嘌呤核苷酸和嘧啶核苷酸的生物合成过程中一碳基团的转移作用受阻,导致DNA的生物合成明显受到抑制。此外,本品也有对胸苷酸合成酶的抑制作用,但抑制RNA与蛋白质合成的作用则较弱。本品主要作用于细胞周期的S期,属细胞周期特异性药物,对G₁/S期的细胞也有延缓作用,对G₁期细胞的作用较弱。
(2)药动学 用量按体表面积小于30mg/m²时,口服吸收良好,1~5小时血药浓度达最高峰;肌内注射后达峰时间为0.5~1小时。血浆蛋白结合率约为50%。本品透过血-脑屏障的量甚微,但鞘内注射后则有相当量可达全身循环。部分经肝细胞代谢转化为多谷氨酸盐,部分通过胃肠道细菌代谢。主要经由肾(40%~90%)排泄,大多以原形药排出体外;≤10%通过胆汁排泄。分布相半衰期(t1/2α)、消除相半衰期(t1/2β)和终末相半衰期(t1/2γ)分别为1小时、2~3小时和8~10小时。小量甲氨蝶呤及其代谢产物可以结合型形式贮存于肾脏和肝脏等组织中,有时可长达数月。在有胸腔或腹腔积液情况下,本品的清除速度明显延迟;清除率个体差别极大,老年患者更甚。
(1)胃肠道反应包括口腔炎、口唇溃疡、咽喉炎、恶心、呕吐、腹痛、腹泻、消化道出血。食欲缺乏常见,偶见假膜性或出血性肠炎等。
(2)肝功能损害包括黄疸、ALT、碱性磷酸酶、γ谷氨酰转肽酶等增高,长期口服可导致肝细胞坏死、脂肪肝、纤维化甚或肝硬化。
(3)大剂量应用时,由于本品和其代谢产物沉积在肾小管而致高尿酸血症性肾病,此时可出现血尿、蛋白尿、尿少、氮质血症甚或尿毒症。
(4)长期用药可引起咳嗽、气短、肺炎或肺纤维化。
(5)骨髓抑制主要引起白细胞和血小板减少,尤以应用大剂量或长期口服小剂量后易引起明显骨髓抑制,甚或贫血和血小板下降而致皮肤或内脏出血。
(6)脱发、皮肤发红、瘙痒或皮疹,后者有时为对本品的过敏反应。
(7)在白细胞低下时可并发感染。
(8)鞘内注射后可能出现视物模糊、眩晕、头痛、意识障碍,甚至嗜睡或抽搐等。
(9)本品的致突变性、致畸形和致癌性较烷化剂为轻,但长期服用后,有潜在的导致继发性肿瘤的危险。
(10)对生殖功能的影响,虽也较烷化剂类抗癌药为小,但确可导致闭经和精子减少或缺乏,尤以长期应用较大剂量后,但一般多不严重,有时呈不可逆性。
妊娠期妇女禁用。
(1)本品的致突变性,致畸性和致癌性较烷化剂为轻,但长期服用后,有潜在的导致继发性肿瘤的危险。
(2)对生殖功能的影响,虽也较烷化剂类抗癌药为小,但确可导致闭经和精子减少或缺乏,尤其是长期应用较大剂量后。但一般多不严重,有时呈不可逆性。
(3)全身极度衰竭、恶病质或并发感染及心肺肝肾功能不全时,禁用本品,周围血象如白细胞低于3.5×109/L或血小板低于50×109/L时不宜用。
(4)有肾病史或发现肾功能异常时,禁用大剂量甲氨蝶呤疗法,未准备好解救药四氢叶酸钙(CF),未充分进行液体补充或碱化尿液时,也不能用大剂量甲氨蝶呤疗法。
(5)大剂量甲氨蝶呤疗法易致严重副反应,须经住院并可能随时监测其血药浓度时才能谨慎使用。滴注时不宜超过6小时,太慢易增加肾脏毒性。大剂量注射本品2~6小时后,可肌内注射甲酰四氢叶酸钙3~6mg,每6小时1次,注射1~4次,可减轻或预防副作用。
(1)乙醇和其他对肝脏有损害药物与本品同用,可增加对肝脏的毒性。
(2)由于用本品后可引起血液中尿酸水平增高,在痛风或高尿酸血症患者应相应增加别嘌醇等剂量。
(3)本品可增加抗凝血作用,甚至引起肝脏凝血因子的缺少或(和)血小板减少症,因此与其他抗凝药同用时宜谨慎。
(4)与保泰松和磺胺类药物同用后,因与蛋白质结合的竞争,可能会引起本品血清浓度的增高而导致毒性反应的出现。
(5)口服卡那霉素可增加口服本品的吸收,而口服新霉素则可减少其吸收。
(6)与弱有机酸和水杨酸盐等同用,可抑制本品的肾排泄而导致血药浓度增高,应酌予减小用量。
(7)氨苯蝶啶、乙胺嘧啶等药物均有抗叶酸作用,如与本品同用可增加其毒副作用。
(8)与氟尿嘧啶同用,或先用氟尿嘧啶后用本品,均可产生拮抗作用,但如先用本品,4~6小时后再用氟尿嘧啶则可产生协同作用。同样本品如与左旋门冬酰胺酶同用也可导致减效,如用后者10日后或于本品用药后24小时内给左旋门冬酰胺酶,则可增效而减少对胃肠道和骨髓的毒副作用。据报道如在用本品前24小时或10分钟后用阿糖胞苷,可增加本品的抗癌活性。本品与放疗或其他骨髓抑制药同用时宜谨慎。
甲氨蝶呤片:2.5mg。
甲氨蝶呤注射液:10ml:1000mg。
注射用甲氨蝶呤:5mg。
(1)取本品约5mg,加0.5%碳酸铵溶液1ml溶解后,用盐酸溶液(9→1000)稀释制成每1ml中含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在244nm与306nm的波长处有最大吸收,在234nm与262nm的波长处有最小吸收。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集108图)一致。
(R)-甲氨蝶呤照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,加流动相溶解并稀释制成每1ml中约含0.2mg的溶液。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液 取消旋甲氨蝶呤,加流动相溶解并稀释制成每1ml中约含40μg的溶液。
色谱条件 用牛血清白蛋白键合硅胶为填充剂;以正丙醇-磷酸盐缓冲液(pH6.9)(取0.71%无水磷酸氢二钠溶液500ml,加0.69%磷酸二氢钠溶液600ml,摇匀,用2mol/L氢氧化钠溶液调节pH值至6.9)(8:92)为流动相;检测波长为302nm;进样体积20μl。
系统适用性 要求系统适用性溶液色谱图中,出峰顺序依次为(S)-甲氨蝶呤峰与(R)-甲氨蝶呤峰,其分离度应大于3.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有(R)-甲氨蝶呤峰,其峰面积不得大于对照溶液主峰面积的3倍(3.0%)。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,加流动相溶解并稀释制成每1ml中含1mg的溶液。
对照溶液 精密量取供试品溶液1ml,置200ml量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液 分别取甲氨蝶呤与叶酸,用流动相溶解并稀释制成每1ml中各约含0.1mg的混合溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以乙腈-7.0%枸橼酸溶液-2.0%无水磷酸氢二钠溶液(8.5:10:80)(用7.0%枸橼酸溶液或2.0%无水磷酸氢二钠溶液调节pH值至6.0)为流动相;检测波长为302nm;系统适用性溶液进样体积10μl,其他溶液进样体积50μl。
系统适用性 要求系统适用性溶液色谱图中,理论板数按甲氨蝶呤峰计算不低于1000,甲氨蝶呤峰与叶酸峰之间的分离度应大于8.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。
限度 供试品溶液色谱图中如有杂质峰,单个杂质的峰面积不得大于对照溶液的主峰面积(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积的4倍(2.0%)。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分不得过12.0%。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取本品0.50g,加25%硫酸镁的硫酸溶液(取硫酸镁25g,加1mol/L硫酸溶液100ml使溶解)4ml,摇匀,置水浴上蒸发至干,于800℃缓缓炽灼至完全炭化,炽灼时间不超过2小时,放冷,依法检查(通则0821第二法),含重金属不得过百万分之五十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.1mg的溶液。
对照品溶液 取甲氨蝶呤对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.1mg的溶液。
色谱条件 见有关物质项下。进样体积10μl。
系统适用性溶液与系统适用性要求见有关物质项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
抗肿瘤药。
遮光,密封,在阴凉处保存。
(R)-甲氨蝶呤

R-2-[4-[N-[(2,4-二氨基-6-蝶啶基)甲基]甲氨基]苯甲酰氨基]戊二酸
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
