登录/
注册
登录/
注册
磷酸可待因
Linsuan Kedaiyin
Codeine Phosphate
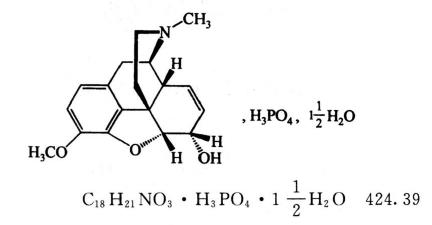
本品为17-甲基-3-甲氧基-4,5α-环氧-7,8-二去氢吗啡喃-6α-醇磷酸盐倍半水合物。按干燥品计算,含C18H21NO3·H3PO4不得少于98.5%。
本品为白色细微的针状结晶性粉末;无臭;有风化性;水溶液显酸性反应。
本品在水中易溶,在乙醇中微溶,在三氯甲烷或乙醚中极微溶解。
①镇咳,用于较剧的频繁干咳,如痰液量较多宜并用祛痰药。②镇痛,用于中度以上的疼痛。③镇静,用于局麻或全麻时。
成人 ①口服或皮下注射∶一次15~30mg,一日30~90 mg。②极量∶口服,一次100mg,一日 250 mg。
【儿科用法与用量】(1)镇痛 口服 一日3mg/kg,分4~6次服。(2)镇咳 口服 剂量为1/3~1/2 镇痛时所用量。【儿科注意事项】 可引起幻觉,呼吸微弱、缓慢或不规则,心律失常。
(1)药效学 对延髓的咳嗽中枢有选择性地抑制,镇咳作用强而迅速;作用于中枢神经系统,兼有镇痛、镇静作用;能抑制支气管腺体的分泌,可使痰液黏稠,难以咳出,故不宜用于多痰及痰液黏稠的患者。
(2)药动学 口服后较易被胃肠吸收,主要分布于肺、肝、肾和胰。本品易于透过血-脑屏障,又能透过胎盘。蛋白结合率一般在 25%左右。半衰期(1/2)约为2.5~4.0小时。镇痛起效时间,口服为30~45分钟,肌内注射和皮下注射为10~30分钟。镇痛最大作用时间,口服为60~120分钟,肌内注射为30~60分钟。作用持续时间,镇痛为4小时,镇咳为4~6小时。经肾排泄,主要为葡糖醛酸结合物。
(1)较多见的不良反应 ①心理变态或幻想。②呼吸微弱、缓慢或不规则。③心率或快或慢、异常。
(2)少见的不良反应 ①惊厥、耳鸣、震颤或不能自控的肌肉运动等。②尊麻疹、瘙痒、皮疹或颜面水肿等过敏反应。③精神抑郁和肌肉强直等。
(3)长期应用可引起依赖性。常用量引起依赖性的倾向较其他吗啡类药为弱。典型的症状为∶鸡皮疙瘩、食欲缺乏、腹泻、牙痛、恶心呕吐、流涕、寒颤、打喷嚏、打呵欠、睡眠障碍、胃痉挛、多汗、衰弱无力、心率增速、情绪激动或原因不明的发热。
(4)逾量时临床表现 头晕、嗜睡、不平静、精神错乱、瞳孔缩小如针尖、癫痫、低血压、心率过缓、呼吸微弱、神志不清。
(1)美国 FDA 妊娠期用药安全性分级为口服给药及肠道外给药C;D(如在临近分娩时长期、大量使用)。本品在妊娠期间可透过胎盘屏障,使胎儿成瘾,引起新生儿的戒断症状如过度啼哭、打喷嚏、打呵欠、腹泻、呕吐等。分娩期应用本品可引起新生儿呼吸抑制。
(2)多痰患者禁用,以防止因抑制咳嗽反射而使痰液阻塞呼吸道,或继发感染而加重病情。
(1)可自乳汁排出,哺乳期妇女慎用。
(2)下列情况应慎用∶①支气管哮喘。②急腹症,在诊断未明确时,可能因掩盖真相造成误诊。③胆结石,可引起胆管痉挛。④原因不明的腹泻,可使肠道蠕动减弱、减轻腹泻症状而误诊。⑤颅脑外伤或颅内病变,本品可引起瞳孔变小、视物模糊的临床症状和体征。⑥前列腺增生症病例,因本品易引起尿潴留而加重病情。
(1)本品与抗胆碱药合用时,可加重便秘或尿潴留的不良反应。
(2)与美沙酮或其他吗啡类药合用时,可加重中枢性呼吸抑制作用。
(3)与肌肉松弛药合用时,呼吸抑制更为显著。
磷酸可待因片∶(1)15mg;(2)30mg。
磷酸可待因糖浆∶(1)10ml∶50 mg;(2)100ml∶500 mg。
磷酸可待因注射液∶(1)1ml∶15mg;(2)1ml∶30 mg。
(1)取本品约0.2g,加水4ml溶解后,在不断搅拌下滴加20%氢氧化钠溶液至出现白色沉淀,用玻璃棒摩擦器壁使沉淀完全,过滤;沉淀用水洗净,在105℃干燥1小时,依法测定(通则0612),熔点为154~158℃。
(2)取本品约0.1g,加水5ml溶解后,滴加氨试液使成碱性,不得生成沉淀。
(3)取本品约1mg,置白瓷板上,加含亚硒酸2.5mg的硫酸0.5ml,立即显绿色,渐变蓝色。
(4)取鉴别(1)项下的沉淀,其红外光吸收图谱应与可待因的对照图谱(光谱集92图)一致。
(5)本品的水溶液显磷酸盐的鉴别反应(通则0301)。
酸度 取本品0.40g,加水10ml溶解后,依法测定(通则0631),pH值应为4.0~5.0。
溶液的澄清度与颜色 取本品0.40g,加新沸过的冷水10ml溶解后,溶液应澄清无色;如显浑浊,与1号浊度标准液(通则0902第一法)比较,不得更浓;如显色,与黄色2号标准比色液(通则0901第一法)比较,不得更深。
氯化物 取本品0.10g,依法检查(通则0801),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.05%)。
硫酸盐 取本品0.20g,依法检查(通则0802),如发生浑浊,与标准硫酸钾溶液2.0ml制成的对照液比较,不得更浓(0.1%)。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含10mg的溶液。
对照品溶液 取吗啡对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含1mg的溶液。
对照溶液 精密量取供试品溶液0.2ml与对照品溶液1ml,置同一100ml量瓶中,用流动相稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以0.03mol/L醋酸钠溶液(用冰醋酸调节pH值至3.5)-甲醇(60∶10)为流动相;检测波长为230nm;进样体积10μl。。
系统适用性要求 对照溶液色谱图中,理论板数按磷酸可待因峰计算不低于2000,吗啡峰与磷酸可待因峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍。
限度 供试品溶液色谱图中如有与吗啡峰保留时间一致的色谱峰,按外标法以峰面积计算,不得过0.1%;其他单个杂质的峰面积不得大于对照溶液中磷酸可待因峰面积的2.5倍(0.5%),各杂质峰面积的和不得大于对照溶液中磷酸可待因峰面积的5倍(1.0%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量应为5.0%~7.5%(通则0831).
取本品约0.25g,精密称定,加冰醋酸10ml溶解后,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显绿色,并将滴定的结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于39.74mg的C18H21NO3·H3PO4。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
