登录/
注册
登录/
注册
来曲唑
Laiquzuo
Letrozole
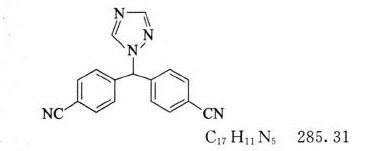
本品为4,4'-(1H-1,2,4-三氮唑-1-基-亚甲基)-二苯腈。按干燥品计算,含C17H11N5应为98.0%~102.0%。
本品为白色或类白色结晶或结晶性粉末;无臭。
本品在丙酮中溶解,在甲醇中微溶,在水和0.1mol/L盐酸溶液中几乎不溶。
熔点本品的熔点(通则0612)为181~185℃。
吸收系数 取本品约10mg,精密称定,加甲醇2ml使溶解,加0.1mol/L盐酸溶液定量稀释制成每1ml中约含5μg的溶液,照紫外-可见分光光度法(通则0401),在240nm的波长处测定吸光度,吸收系数(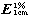 )为1150~1222。
)为1150~1222。
①用于绝经后雌激素受体阳性、孕激素受体阳性或受体状况不明的晚期乳腺癌患者,这些患者应为自然绝经或人工诱导绝经。②用于绝经后雌激素受体及孕激素受体阳性的乳腺癌患者手术后辅助治疗。
口服一次2.5mg,一日1次。可在三餐的餐前、餐后或进餐同时服用。
(1)药效学 本品是一种高选择性非甾体类芳香化酶抑制剂。通过竞争性地与细胞色素P450酶亚单位的血红素结合,从而抑制芳香化酶,导致雌激素在所有组织中的生物合成减少。在健康绝经后女性中,单次应用0.1mg、0.5mg、2.5mg的本品,可以分别从基线水平将雌酮和雌二醇的血清浓度降低75%~78%和78%。在48~78小时可达到最强效果。在绝经后晚期乳腺癌患者中,所有接受一日0.1~5mg剂量的患者,其血浆雌二醇、雌酮水平可以分别从基线水平下降75%~95%,抑制雌激素对肿瘤生长的刺激作用。未观察到对肾上腺皮质激素合成的抑制作用。因此,不必补充糖皮质激素和盐皮质激素。本品抑制雌激素的生物合成并不会导致雄激素前体的聚集。本品对血浆黄体生成素(LH)和促卵泡刺激素(FSH)水平亦无负面影响,通过促甲状腺激素(TSH)、四碘甲状腺原氨酸(T4)和三碘甲状腺原氨酸(T3)的摄取实验证实,它同样不会对甲状腺功能产生影响。
(2)药动学 本品口服后在胃肠道吸收迅速、完全。生物利用度达99.9%,与食物同服可轻度降低本品的吸收速率,但不影响吸收程度。口服后1小时达血药浓度峰值。服药2~6周达到血浆稳态浓度。本品在组织中分布迅速、广泛,稳态时的表观分布容积为(1.87±0.47)L/kg。本品60%与血浆蛋白结合,主要是清蛋白(55%)。本品主要的消除途径是转变为无药理活性的葡糖醛酸化的甲醇代谢物(清除率=2.1L/h)。本品通过肾脏排泄,主要是代谢产物和约6%的原形药。终末相半衰期(t1/2γ)为75~110小时。
(1)主要为轻度或中度的恶心、骨关节痛、潮热、疲倦和体重增加。
(2)其他反应便秘、腹泻、瘙痒、皮疹、头疼、背痛、胸痛、腹痛、乳房痛、失眠、头晕、水肿、高血压、心律失常、血栓形成、呼吸困难、阴道流血等,较少见。
(1)对本品过敏的患者禁用。
(2)妊娠期和哺乳期妇女禁用。
(3)儿童禁用。
(1)肝功能和(或)肾功能不全(肌酐清除率≥10ml/min)者无须调整剂量,尚无肌酐清除率<10ml/min女性患者用药临床资料。
(2)服用时可不考虑进食时间,即来曲唑可在进食前、后或同时服用。
(3)老年患者无须调整剂量。
(4)本品对患者驾驶和机械操作能力无明显影响,但若服药过程中出现疲乏和头晕时,应提醒注意。
经细胞色素P450(CYP)3A4酶代谢的药物有可能影响本品的生物转化。与经CYP2C19酶代谢的药物合用时应非常谨慎,而与经CYP2A6酶代谢的药物合用时不太可能产生临床相互作用。尚无与其他抗肿瘤药物合用的临床资料。
来曲唑片:2.5mg。
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取吸收系数项下溶液,照紫外-可见分光光度法(通则0401)测定,在240nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集953图)一致。
有关物质照高效液相色谱法(通则0512)测定。
溶剂乙腈-水(30∶70)。
供试品溶液取本品约20mg,精密称定,置200ml量瓶中,加溶剂溶解并稀释至刻度,摇匀。
对照溶液 精密量取供试品溶液适量,用溶剂定量稀释制成每1ml中含0.1μg的溶液。
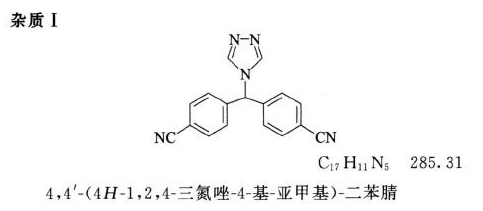
系统适用性溶液 取来曲唑系统适用性对照品(含杂质Ⅰ)适量,加乙腈溶解后,用溶剂稀释制成每1ml约含来曲唑0.1mg的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(ZorbaxSB-C18,4.6mmX150mm,5μm或效能相当的色谱柱);以水为流动相A,乙腈为流动相B,按下表进行线性梯度洗脱;检测波长为230nm;进样体积20μl。
时间(分钟) 流动相A(%) 流动相B(%)
0 70 30
25 30 70
25.1 70 30
30 70 30
系统适用性 要求系统适用性溶液色谱图中,来曲唑峰的保留时间为8~10分钟,杂质Ⅰ峰(相对保留时间约为0.67)与来曲唑峰的分离度应不小于5.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,杂质Ⅰ的峰面积不得大于对照溶液主峰面积的3倍(0.3%),其他单个杂质峰面积不得大于对照溶液的主峰面积(0.1%),其他杂质峰面积的和不得大于对照溶液主峰面积的3倍(0.3%),小于对照溶液主峰面积0.5倍的峰忽略不计(0.05%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品约25mg,精密称定,置50ml量瓶中,加乙腈15ml,振摇使溶解,用水稀释至刻度,摇匀;精密量取2ml,置100ml量瓶中,加溶剂稀释至刻度,摇匀。
对照品溶液 取来曲唑对照品约25mg,精密称定,置50ml量瓶中,加乙腈15ml,振摇使溶解,用水稀释至刻度,摇匀;精密量取2ml,置100ml量瓶中,加溶剂稀释至刻度,摇匀。
溶剂、系统适用性溶液、色谱条件与系统适用性要求见有关物质项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
抗肿瘤药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
