登录/
注册
登录/
注册
乌苯美司
Wubenmeisi
Wubenmeisi
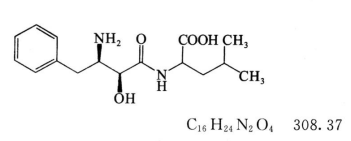
本品为N-[(2S,3R)-3-氨基-2-羟基-4-苯基丁酰]-L-亮氨酸。按干燥品计算,含C16H24N2O4不得少于98.5%。
本品为白色结晶性粉末;无臭。
本品在水或甲醇中微溶;在冰醋酸中易溶,在0.1mol/L盐酸溶液或0.1mol/L氢氧化钠溶液中溶解。
比旋度 取本品,精密称定,加0.1mol/L盐酸溶液溶解并定量稀释制成每1ml中约含10mg的溶液,依法测定(通则0621),比旋度为-15.5°至-17.5°。
①本品可增强免疫功能,用于抗癌化疗、放疗的辅助治疗,老年性免疫功能缺陷等。②可配合化疗、放疗和联合应用于白血病、多发性骨髓瘤、骨髓增生异常综合征及造血干细胞移植后,以及其他实体瘤患者。
成人,一日30mg,1次(早晨空腹口服)或分3次口服;儿童酌减。症状减轻或长期服用,也可每周服用2~3次,10个月为一疗程。
(1)药效学 本品从链霉菌属(Streptomyesofiwreticuli)的培养液中分离所得的二肽化合物,可竞争性地抑制氨肽酶B(aminopeptidaseB)及亮氨酸肽酶(leucineaminopeptidase)。增强T细胞的功能,使NK细胞的杀伤活力增强,且可使集落刺激因子合成增加而刺激骨髓细胞的再生及分化。抗肿瘤作用机制尚不十分明确,可能干扰肿瘤细胞的代谢,抑制肿瘤细胞增生,使肿瘤细胞凋亡,并激活人体细胞免疫功能,刺激细胞因子的生成和分泌,促进抗肿瘤效应细胞的产生和增殖。
(2)药动学 本品口服吸收良好、迅速,1小时后血药浓度可达峰值。本品约有15%在肝中被代谢为羟基乌苯美司。给药量的80%~85%以原形自尿排出。
(1)偶有皮疹、瘙痒、头痛、面部浮肿和一些消化道反应,如恶心、呕吐、腹泻、软便。个别服用者可出现氨基转移酶(AST、ALT)升高,均属轻度,一般在口服过程中或停药后消失。
(2)日本对2164例用药者(上市前考察939例,上市后考察1225例)的不良反应进行统计,不良反应及临床实验室检查值异常的发生率约为4.2%,不良反应发生率仅为2.3%,主要为肝功能损害异常(AST、ALT)上升约占1.8%,皮肤异常(出疹、发红、瘙痒感等)约为1.3%、消化道异常(恶心、呕吐、食欲缺乏等)约为0.9%。
其他少见的不良反应包括肝脏AST上升、ALT上升、皮疹、发红、瘙痒感、脱毛、恶心、呕吐、食欲缺乏、腹痛、腹部饱胀感、腹泻、头痛、颜抖感、麻痹感其他口腔内异样感、浮肿。
乌苯美司片:10mg。
乌苯美司胶囊:10mg。
(1)取本品约10mg,加20%醋酸溶液2ml、茚三酮约5mg与1mol/L氢氧化钠溶液2滴,加热,溶液渐显蓝紫色。
(2)取本品和乌苯美司对照品各适量,加有关物质项下的流动相A分别溶解并稀释制成每1ml中各约含0.3mg的供试品溶液与对照品溶液,照有关物质项下的色谱条件试验,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)取本品适量,加水溶解并稀释制成每1ml中约含0.5mg的溶液,照紫外-可见分光光度法(通则0401)测定,在252nm、257nm与263nm的波长处有最大吸收,在254nm与261nm的波长处有最小吸收。
(4)本品的红外光吸收图谱应与对照的图谱(光谱集911图)一致。
酸度 取本品0.25g,加水25ml,振摇,滤过,取滤液,依法测定(通则0631),pH值应为4.5-7.0。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,加流动相A溶解并稀释制成每1ml中约含3mg的溶液。
对照溶液 精密量取供试品溶液适量,用流动相A定量稀释制成每1ml中约含15μg的溶液。
灵敏度溶液 精密量取对照溶液适量,用流动相A定量稀释制成每1ml中约含1.5μg的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以65mmol/L磷酸二氢钾溶液-乙腈(17:3)为流动相A,乙腈-65mmol/L磷酸二氢钾溶液(2:1)为流动相B,按下表进行梯度洗脱;柱温25℃;检测波长220nm;进样体积20μl。

系统适用性 要求对照溶液色谱图中,理论板数按乌苯美司峰计算不低于5000;灵敏度溶液色谱图中,乌苯美司色谱峰的信噪比应不小于10。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积的2倍(1.0%),供试品溶液色谱图中小于灵敏度溶液主峰面积的色谱峰忽略不计(0.05%)。
残留溶剂照残留溶剂测定法(通则0861)测定,应符合规定。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
取本品约0.25g,精密称定,加冰醋酸30ml使溶解,照电位滴定法(通则0701),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于30.84mg的C16H24N2O4。
免疫调节药,抗肿瘤药。
密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
