登录/
注册
登录/
注册
盐酸昂丹司琼
YansuanAngdansiqiong
OndansetronHydrochloride
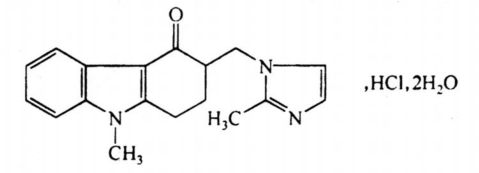
C18H19N3O・HCl・2H2O 365.86
本品为2,3-二氢-9-甲基-3-[(2-甲基咪唑-1-基)甲基]-4(1H)-咔唑酮盐酸盐二水合物。按无水物计算,含C18H19N3O・HCl应为98.0%~102.0%。
本品为白色或类白色结晶性粉末;无臭。
本品在甲醇中易溶,在水中略溶,在丙酮中微溶;在0.1mol/L盐酸溶液中略溶。
熔点 取本品,以五氧化二磷为干燥剂干燥30分钟后,依法测定(通则0612),熔点为175~180℃,熔融时同时分解。
止吐药。用于:①细胞毒性药物化疗和放射治疗引起的恶心呕吐;②预防和治疗手术后的恶性呕吐。
成人一日8mg。
(1)对于高度催吐的化疗药引起的呕吐在化疗前30分钟,化疗后4小时、8小时各静脉滴注本品8mg,停止化疗以后每8~12小时口服片剂8mg。
(2)对催吐程度不太强的化疗药引起的呕吐,化疗前30分钟静脉滴注本品8mg,以后每8~12小时口服片剂8mg,连用5天。
(3)对于放射治疗引起的呕吐,首剂应于放疗前1~2小时口服片剂8mg,以后每8小时口服8mg。
(4)对于预防和治疗手术后呕吐,成人可于麻醉诱导同时静脉滴注本品4mg,对已出现术后恶心呕吐时,可缓慢静脉滴注本品4mg进行治疗。输注时间应不小于15分钟。
(1)药效学 本品是一强效、高选择性的5-羟色胺(5-HT3)受体拮抗药,有强镇吐作用。药物化疗和放射治疗可造成小肠释放5-羟色胺(5-HT),经由5-HT3受体激活迷走神经的传入支,触发呕吐反射。一般认为,本品能阻断此处的5-HT3受体而发挥止吐作用的。由于本品的高选择性作用,因而不具有其他止吐药的副作用,如锥体外系反应、过度镇静等。
(2)药动学 本品口服后血药浓度达峰时间为1.5小时,其生物利用度约为60%(老年人则更高),血浆蛋白结合率为75%。口服或静脉给药时,本品的体内情况大致相同,消除相半衰期(t1/2β)为3小时,老年人可能延长至5小时。药物彻底代谢,代谢物经肾脏(75%)与肝脏(25%)排泄。
可有头痛,头部和上腹部有温热感,腹部不适、便秘、口干、皮疹、注射部位局部反应,偶见支气管哮喘或过敏反应,暂时性无症状转氨酶升高。上述反应一般轻微,不需特殊处理。偶见运动失调,癫痛发作,胸痛、心律不齐、低血压及心动过缓等罕见报告。
对本品过敏者禁用。胃肠梗阻者禁用。
(1)妊娠期妇女及哺乳期妇女慎用。
(2)胃肠道梗阻者不宜应用。
盐酸昂丹司琼片:(1)4mg;(2)8mg。
盐酸昂丹司琼胶囊:(1)4mg;(2)8mg。
盐酸昂丹司琼注射液:(1)2ml:4mg;(2)4ml:8mg。
(1)取本品约10mg,加水5ml使溶解,加稀碘化铋钾试液1ml,即生成猩红色沉淀。
(2)取本品,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在248nm、267nm与310nm的波长处有最大吸收,在282nm与257nm的波长处有最小吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集832图)一致。
(4)本品显氯化物的鉴别反应(通则0301)。
酸度 取本品0.10g,加水10ml溶解后,依法测定(通则0631),pH值应为4.0~5.5。
溶液的澄清度与颜色 取本品0.10g,加水10ml溶解后,溶液应澄清无色。如显浑浊,与1号浊度标准液(通则0902第一法)比较,不得更浓;如显色,与黄色1号标准比色液(通则0901第一法)比较,不得更深。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,加流动相溶解并稀释制成每1ml中约含0.5mg的溶液。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
色谱条件 用氰基硅烷键合硅胶为填充剂;以0.02mol/L磷酸二氢钠溶液(用氢氧化钠试液调节pH值至5.4)-乙腈(50∶50)为流动相;检测波长为216nm;进样体积10μl。
系统适用性要求理论板数按昂丹司琼峰计算不低于2000。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。
限度 供试品溶液色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液主峰面积的0.5倍(0.5%)。
残留溶剂照残留溶剂测定法(通则0861第三法)测定。
供试品溶液 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含20mg的溶液。
对照品溶液 取甲苯与丙酮各适量,精密称定,加水定量稀释制成每1ml中约含17.8μg与100μg的溶液。
色谱条件 以5%苯基-95%甲基聚硅氧烷毛细管柱为色谱柱;柱温为50℃;进样体积1~3μl。
系统适用性 要求对照品溶液色谱图中,甲苯峰与丙酮峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入气相色谱仪,记录色谱图。
限度 按外标法以峰面积计算,甲苯与丙酮的残留量均应符合规定。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分应为9.0%~10.5%。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之二十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.1mg的溶液。
对照品溶液 取盐酸昂丹司琼对照品,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.1mg的溶液。
色谱条件与系统适用性要求见有关物质项下。检测波长为310nm。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
抗肿瘤辅助药。
遮光,密封保存。
杂质Ⅰ
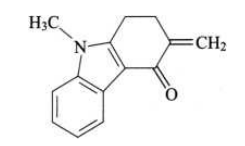
C14H13NO 211.26
9-甲基-3-亚甲基-2,3-二氢-1H-咔唑-4(9H)-酮
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
