登录/
注册
登录/
注册
芬布芬
Fenbufen
Fenbufen
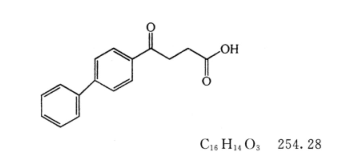
本品为3-(4-联苯基羰基)丙酸。按干燥品计算,含C16H14O3不得少于98.5%。
本品为白色或类白色结晶性粉末;无臭。
本品在乙醇中溶解,在水中几乎不溶;在热碱溶液中易溶。
熔点本品的熔点(通则0612)为185~188℃。
本品用于类风湿关节炎、风湿性关节炎、骨关节炎、脊柱关节病、痛风性关节炎的痛肿治疗。还可用于牙痛、手术后疼痛及外伤性疼痛的止痛。
口服成人一日0.6g,1次或分2次服用。成人每日总量不超过1.0g。
(1)药效学 本品为一种长效的NSAIDs。本身属前体药,进入体内后代谢成为联苯乙酯后具有抑制环氧酶的活性,使前列腺素的合成减少而起作用。动物实验表明,本品的抗炎镇痛作用比吲哚美辛弱,但比阿司匹林强。
(2)药动学 本品口服后2小时左右80%被吸收。在肝内代谢为具有活性的联苯乙酯。活性物质的血浓度在6~8小时达峰值。t1/2较长,约7小时,但72小时仍在血中可以测到浓度。98%~99%与血浆蛋白结合。66%由尿排出,10%则呼出体外,10%由粪便排出。
本品不良反应主要为胃肠反应,表现为胃痛、胃烧灼感、恶心,发生率约12%~13%,少数(2%)出现严重不良反应包括胃溃疡、出血甚至穿孔。头晕、皮疹、白细胞数轻度下降、氨基转移酶微升等较少见。
(1)消化性溃疡,严重肝、肾功能损害,阿司匹林引起哮喘者禁用。
(2)妊娠期妇女、哺乳期妇女禁用。
(3)对本品或其他NSAIDs过敏者禁用。
交叉过敏反应,同其他NSAIDs。
(1)饮酒或与其他NSAIDs同用时增加胃肠道不良反应,并有致溃疡的危险。长期与对乙酰氨基酚同用时可增加对肾脏的不良反应。
(2)与阿司匹林或其他水杨酸类药物同用时,药效不增强,而胃肠道不良反应及出血倾向发生率增高。
(3)与肝素、双香豆素等抗凝药及血小板聚集抑制药同用时有增加出血的危险。
(4)与呋塞米同用时,后者的排钠和降压作用减弱。
(5)与维拉帕米、硝苯地平同用时,本品的血药浓度增高。
(6)本品可增加地高辛的血药浓度,同用时须注意调整地高辛的剂量。
(7)本品可增强抗糖尿病药(包括口服降糖药)的作用。
(8)本品与抗高血压药同用时可影响后者的降压效果。
(9)丙磺舒可降低本品的排泄,增加血药浓度,从而增加毒性,故同用时宜减少本品剂量。
(10)本品可降低甲氨蝶呤的排泄,增加其血浓度,甚至可达中毒水平,故本品不应与中或大剂量甲氨蝶呤同用。
(11)药物的不良反应与所服用的剂量呈正相关,因此服药超量时应做紧急处理,包括催吐或洗胃、口服活性炭、抗酸药或(和)利尿药,并给予监测及其他支持疗法。
(12)本品可增加喹诺酮类抗感染药物的中枢副作用。
芬布芬片:(1)0.15g;(2)0.3g。
芬布芬胶囊:(1)0.15g;(2)0.2g。
(1)取本品约0.1g,加硫酸2ml,溶液显橙红色,加水稀释后,颜色即消失,并生成白色沉淀。
(2)取本品约0.1g,加无水乙醇5ml,加热使溶解,放冷,滴加三氯化铁试液,即生成橘黄色沉淀。
(3)取本品,加无水乙醇制成每1ml中约含5μg的溶液,照紫外-可见分光光度法(通则0401)测定,在281nm的波长处有最大吸收,在238nm的波长处有最小吸收。
(4)本品的红外光吸收图谱应与对照的图谱(光谱集170图)一致。
氯化物 取无水碳酸钠2g,铺于坩埚底部和四周,再取本品1.0g,置无水碳酸钠上,用少量水湿润,干燥后,先用小火炽灼使炭化,再在700~800℃炽灼使完全灰化,放冷,加水适量使溶解,滤过,坩埚和滤器用水洗涤,合并滤液与洗液,置50ml量瓶中,用水稀释至刻度,摇匀,精密量取10ml,加水使成25ml,依法检查(通则0801),与标准氯化钠溶液6.0ml用同一方法制成的对照液比较,不得更深(0.03%)。
硫酸盐 取上述氯化物项下剩余的滤液10.0ml,加水使成25ml,依法检查(通则0802),与标准硫酸钾溶液2.0ml用同一方法制成的对照液比较,不得更深(0.1%)。
有关物质照高效液相色谱法(通则0512)测定。
溶剂1.8%冰醋酸溶液-乙腈(68:32)。
供试品溶液 取本品约50mg,置25ml量瓶中,加N,N-二甲基甲酰胺10ml,振摇使溶解,用溶剂稀释至刻度,摇匀。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用溶剂稀释至刻度,摇匀。
系统适用性溶液 取芬布芬与酮洛芬对照品各适量,加溶剂溶解并稀释制成每1ml中约含芬布芬0.02mg与酮洛芬0.05mg的混合溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;流动相A为1.8%冰醋酸溶液,流动相B为乙腈,按下表进行梯度洗脱;流速为每分钟1.5ml;检测波长为283nm;柱温为30℃;进样体积20μl。
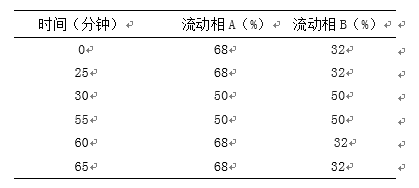
系统适用性 要求系统适用性溶液色谱图中,酮洛芬峰与芬布芬峰之间的分离度应大于5.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(1.0%),各杂质峰面积的和不得大于对照溶液主峰面积的2倍(2.0%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过1.0%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
砷盐 取上述氯化物项下剩余的滤液10.0ml,加盐酸5ml与水13ml,依法检查(通则0822第一法),应符合规定(0.001%)。
取本品0.4g,精密称定,加中性乙醇50ml,置热水中使溶解,放冷,加酚酞指示液2滴,用氢氧化钠滴定液(0.1mol/L)滴定。每1ml氢氧化钠滴定液(0.1mol/L)相当于25.43mg的C16H14O3。
解热镇痛、非甾体抗炎药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
