登录/
注册
登录/
注册
羟苯磺酸钙
Qiangbenhuangsuangai
CalciumDobesilate
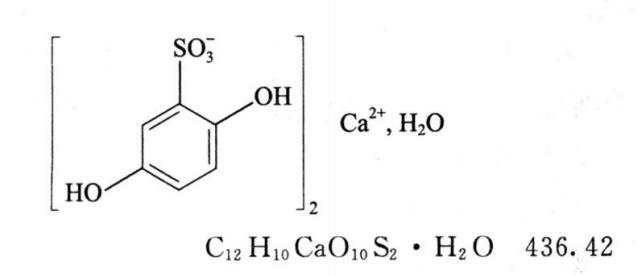
本品为2,5-二羟基苯磺酸钙一水合物,按无水与无溶剂物计算,含C12H10CaO10S2应为99.0%~102.0%。
本品为白色或类白色粉末;无臭;遇光易变质,有吸湿性。
本品极易溶于水,易溶于乙醇或丙酮,极微溶于三氯甲烷或乙醚。
用于糖尿病性视网膜病变。
口服①亚临床视网膜病变或预防性用药:一日0.5g,分1~2次服用;②非增生性视网膜病变或隐匿性视网膜病变:一日0.75~1.5g,分2~3次服用;③增生性视网膜病变:一日1.5~2g,分3~~4次服用。
轻症疗程为1~3个月,中症疗程为6~12个月,重症疗程为1~2年。
(1)药效学 本品能调整和改善毛细血管壁的通透性和柔韧性,拮抗诱导血管通透性增加的活性物质(如组胺、5-羟色胺、缓激肽、透明质酸酶、前列腺素、血小板激活因子)及防止胶原的改变。对血液高黏稠度,本品通过降低大分子血浆蛋白、纤维蛋白原和球蛋白的水平,调节清蛋白与球蛋白的比值,增强红细胞的柔韧性和降低它们的高聚性。此外,还能激活纤维蛋白溶解,从而使血液黏滞性降低。对血小板高聚性,本品可减少血小板聚集因子的合成和释放,明显抑制多种聚集因子(如β-凝血蛋白、血栓素A₂、血小板激活因子等)引起的聚集反应和血小板自发性聚集反应,还能抑制二磷酸腺苷诱导的血栓形成。此外还能改善淋巴液的回流。
(2)药动学 口服给药500mg,血药浓度达峰时间和峰值分别为6小时和8mg/L,血浆蛋白结合率为20%~25%,消除相半衰期为1.23小时。本品除不能通过血-脑屏障外,可全身性分布。口服24小时经尿排出量50%,其中10%以代谢物形式排出,部分经粪便排泄。
长期服用本品通常耐受性较好。
(1)较大剂量时,极少数患者可有胃部不适、灼热、恶心、食欲缺乏等胃肠道反应。
(2)可见皮肤过敏反应,如荨麻疹。
(3)偶见发热、出汗、脸部红热、心脏不适等。
(1)对本品过敏者禁用。
(2)儿童禁用。
(1)使用本品需结合降糖药进行治疗,第一次使用本品前应咨询医师。
(2)治疗期间应定期到医院检查。
(3)妊娠前3个月及哺乳期妇女不推荐使用。
(4)胃肠功能障碍者慎用。
(5)老年患者慎用。
禁与抗凝血药物联用,以免增强羟苯磺酸钙的作用。
羟苯磺酸钙片:0.5g。
羟苯磺酸钙胶囊:(1)0.25g;(2)0.5g。
(1)取本品约0.1g,置试管中,加乙醇2ml溶解,滴加三氯化铁试液2滴,显蓝色,放置后变为蓝紫色。
(2)取本品约0.1g,加水2ml溶解,将溶液分为2份,一份加硝酸1ml,水浴中加热15~20分钟,放冷,加氯化钡试液1ml,立即产生白色沉淀;另一份加硝酸1滴,再加氯化钡试液1ml,无沉淀产生。
(3)取本品,加水溶解并稀释制成每1ml中约含25μg的溶液,照紫外-可见分光光度法(通则0401)测定,在221nm与301nm的波长处有最大吸收。
(4)本品的水溶液显钙盐的鉴别反应(通则0301)。
酸度 取本品,加水溶解并稀释制成每lml中含0.1g的溶液,依法测定(通则0631),pH值应为4.5~6.0。
溶液的澄清度与颜色 取本品1.0g,加水10ml溶解后,溶液应澄清无色;如显浑浊,与1号浊度标准液(通则0902第一法)比较,不得更浓;如显色,与黄色1号标准比色液(通则0901第一法)比较,不得更深。
硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液3.0ml制成的对照液比较,不得更浓(0.03%)。
有关物质照高效液相色谱法(通则0512)测定。避光操作。
供试品溶液 取本品,精密称定,加水溶解并定量稀释制成每1ml中约含1mg的溶液。
对照溶液 精密量取供试品溶液适量,用水定量稀释制成每1ml中约含1μg的溶液。
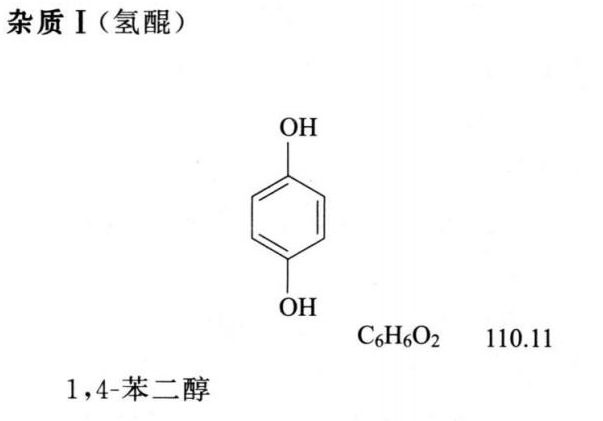
对照品溶液 取杂质I对照品,精密称定,加水溶解并定量稀释制成每1ml中约含1μg的溶液。
系统适用性溶液 取羟苯磺酸钙与杂质I对照品各适量,加水溶解制成每1ml中分别约含100μg与1μg的混合溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以乙腈-0.05mol/L磷酸二氢铵溶液(2:98)为流动相;检测波长为300nm;进样体积10μl。
系统适用性 要求系统适用性溶液色谱图中,理论板数按羟苯磺酸钙峰计算不低于1000,羟苯磺酸钙峰与杂质I峰之间的分离度应符合要求。
测定法 精密量取供试品溶液、对照溶液与对照品溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。
限度 供试品溶液色谱图中,如有与杂质I峰保留时间一致的色谱峰,按外标法以峰面积计算,不得过0.1%;其他单个杂质峰面积不得大于对照溶液的主峰面积(0.1%);杂质总量不得过0.2%。
残留溶剂照残留溶剂测定法(通则0861第二法)测定。
内标溶液 取正丙醇,用水稀释制成每1ml中约含120μg的溶液。
供试品溶液 取本品约0.2g,精密称定,置顶空瓶中,精密加入内标溶液2ml使溶解,密封。
对照品溶液 取乙醇、异丙醇和1,2-二氯乙烷各适量,精密称定,加内标溶液定量稀释制成每1ml中约含乙醇500μg、异丙醇500μg和1,2-二氯乙烷0.5μg的混合溶液,精密量取2ml,置顶空瓶中,密封。
色谱条件 以6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液;起始温度为40℃,维持5分钟,以每分钟10℃的速率升温至150℃,保持2分钟,以每分钟20℃的速率升温至240℃,维持3分钟;进样口温度为230℃;检测器温度为250℃;顶空瓶平衡温度为70℃,平衡时间为30分钟。
系统适用性 要求对照品溶液色谱图中,各成分峰之间的分离度均应符合要求。
测定法 取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度 按内标法以峰面积计算,乙醇、异丙醇与1,2-二氯乙烷的残留量均应符合规定。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分应为4.0%~6.0%。
铁盐 取本品1.0g,依法检查(通则0807),与标准铁溶液1.0ml制成的对照液比较,不得更深(0.001%)。
重金属 取本品1.0g,加水适量溶解后,加醋酸盐缓冲液(pH3.5)2ml,用水稀释至25ml,依法检查(通则0821第一法),含重金属不得过百万分之十五。
取本品约0.2g,精密称定,加水10ml使溶解,加稀硫酸40ml与邻二氮菲指示液2滴,用硫酸铈滴定液(0.1mol/L)滴定至溶液显黄绿色。每1ml硫酸铈滴定液(0.1mol/L)相当于10.46mg的C12H10CaO10S2。
毛细血管保护药。
密封,在凉暗、干燥处保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
