登录/
注册
登录/
注册
葛根素注射液
GegensuZhusheye
PuerarinInjection
本品为葛根素加适量助溶剂制成的灭菌水溶液。含葛根素(C21H20O9)应为标示量的93.0%~107.0%。
本品为无色至微黄色的澄明液体。
(1)取本品适量,加0.5%三氯化铁溶液2~3滴,摇匀,再加0.5%铁氰化钾溶液2~3滴,摇匀,显蓝绿色。
(2)取本品适量,加乙醇制成每1ml中约含葛根素10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在250nm的波长处有最大吸收。
pH值应为3.5~5.5(通则0631)。
溶液的颜色 取本品,与黄色2号标准比色液(通则0901第一法)比较,不得更深。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,用溶剂稀释制成每1ml中约含葛根素0.5mg的溶液。
对照溶液 精密量取供试品溶液适量,用溶剂定量稀释制成每1ml中约含5μg的溶液。
系统适用性要求 见葛根素有关物质项下。供试品溶液色谱图中,杂质Ⅰ峰与杂质Ⅱ峰的相对保留时间约为2.0与2.2(必要时用如下方法确认:取葛根素对照品20mg,置20ml顶空瓶中,加水10ml,水浴加热使溶解,密封,于121℃高压蒸汽破坏20分钟,放冷,量取5ml,置20ml量瓶中,用溶剂稀释至刻度,摇匀,取10μl,注入液相色谱仪,在葛根素峰后应有两个明显的色谱峰,相对保留时间约为2.0与2.2)。
溶剂、系统适用性溶液、色谱条件与测定法 见葛根素有关物质项下。
限度 供试品溶液色谱图中如有杂质峰,杂质Ⅰ与杂质Ⅱ的峰面积均不得大于对照溶液主峰面积的1.5倍(1.5%),其他单个杂质峰面积不得大于对照溶液主峰面积的0.5倍(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积的3倍(3.0%)。
丙二醇 照气相色谱法(通则0521)测定。
供试品溶液 精密量取本品1ml,置100ml量瓶中,用甲醇稀释至刻度,摇匀,精密量取5ml,置50ml量瓶中,用甲醇稀释至刻度,摇匀。
对照品溶液 取丙二醇对照品适量,精密称定,用甲醇定量稀释制成每1ml中约含0.5mg的溶液。
系统适用性溶液 取丙二醇、1,3-丙二醇与二甘醇对照品各适量,精密称定,用甲醇稀释制成每1ml中各含0.5mg的混合溶液。
色谱条件 用聚乙二醇20M(或极性相近)为固定液;初始温度为50℃,以每分钟30℃的速率升温至220℃,维持5分钟;进样口温度为250℃;检测器温度为280℃;进样体积1μl。
系统适用性要求 系统适用性溶液色谱图中,各组分出峰顺序为:丙二醇、1,3-丙二醇、二甘醇,各组分峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入气相色谱仪,记录色谱图。
限度 按外标法以峰面积计算,每1ml中含丙二醇不得过550mg。
二甘醇 照气相色谱法(通则0521)测定。
供试品溶液 取本品5g,精密称定,置10ml量瓶中,用甲醇稀释至刻度,摇匀。
对照品溶液 取二甘醇对照品适量,精密称定,用甲醇定量稀释制成每1ml中约含5μg的溶液。
系统适用性溶液、色谱条件、系统适用性要求与测定法 见丙二醇项下。
限度 按外标法以峰面积计算,含二甘醇不得过0.001%。
异常毒性 取本品,加氯化钠注射液制成每1ml中含葛根素10mg的溶液,依法检查(通则1141),应符合规定。
热原 取本品5ml,加无热原氯化钠注射液制成每1ml中含葛根素10mg的溶液,依法检查(通则1142),剂量按家兔体重每1kg缓缓注射5ml,应符合规定。
过敏反应取本品,依法检查(通则1147),应符合规定。
溶血与凝聚 取本品,加氯化钠注射液制成每1ml中含葛根素20mg的溶液,依法检查(通则1148),应符合规定。
其他 应符合注射剂项下有关的各项规定(通则0102)。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,用流动相定量稀释制成每1ml中约含葛根素50μg的溶液。
对照品溶液、色谱条件、系统适用性要求与测定法 见葛根素含量测定项下。
(1)2ml:50mg(2)2ml:100mg
血管扩张药。
遮光,密闭保存。
杂质Ⅰ
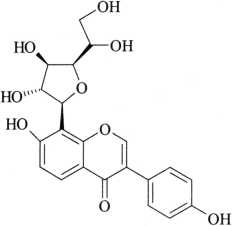
C21H20O9 416.38
8-(β-D-呋喃葡萄糖-1-基)-4',7-二羟基异黄酮
杂质Ⅱ
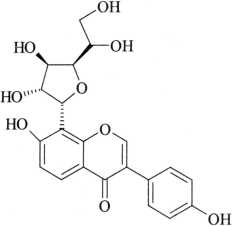
C21H20O9 416.38
8-(α-D-呋喃葡萄糖-1-基)-4',7-二羟基异黄酮
中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
