登录/
注册
登录/
注册
清开灵注射液
Qingkailing Zhusheye
胆酸3.25g 珍珠母(粉)50.0g
猪去氧胆酸3.75g 栀子25.0g
水牛角(粉)25.0g 板蓝根200.0g
黄芩苷5.0g 金银花60.0g
以上八味,板蓝根加水煎煮二次,每次1小时,合并煎液,滤过,滤液浓缩至200ml,加乙醇使含醇量达60%,冷藏,滤过,滤液回收乙醇,加水,冷藏备用。栀子加水煎煮二次,第一次1小时,第二次0.5小时,合并煎液,滤过,滤液浓缩至25ml,加乙醇使含醇量达60%,冷藏,滤过,滤液回收乙醇,加水,冷藏备用。金银花加水煎煮二次,每次0.5小时,合并煎液,滤过,滤液浓缩至60ml,加乙醇使含醇量达75%,滤过,滤液调节pH值至8.0,冷藏,回收乙醇,再加乙醇使含醇量达85%,冷藏,滤过,滤液回收乙醇,加水,冷藏备用。水牛角粉用氢氧化钡溶液、珍珠母粉用硫酸分别水解7~9小时,滤过,合并滤液,调节pH值至3.5~4.0,滤过,滤液加乙醇使含醇量达60%,冷藏,滤过,滤液回收乙醇,加水,冷藏备用。将栀子液、板蓝根液和水牛角、珍珠母水解混合液合并后,加到胆酸、猪去氧胆酸的75%乙醇溶液中,混匀,加乙醇使含醇量达75%,调节pH值至7.0,冷藏,滤过,滤液回收乙醇,加水,冷藏备用。黄芩苷用注射用水溶解,调pH值至7.5,加入金银花提取液,混匀,与上述各备用液合并,混匀,并加注射用水至1000ml,再经活性炭处理后,冷藏,灌封,灭菌,即得。
本品为棕黄色或棕红色的澄明液体。
清热解毒,化痰通络,醒神开窍。用于热病,神昏,中风偏瘫,神志不清;急性肝炎、上呼吸道感染、肺炎、脑血栓形成、脑出血见上述证候者。
1.外感发热 外感温热邪毒所致。症见高热烦躁,口渴饮冷,胸闷咳喘,痰多色黄,甚至神昏谵语,四肢抽搐,角弓反张,或斑疹,吐衄,舌绛苔黄,脉数;上呼吸道感染、肺炎、流脑、乙脑见上述证候者。
2.中风 热毒内盛,痰阻清窍所致。症见突然昏倒,不省人事,半身不遂,口舌歪斜.言语不利,牙关紧闭,面赤气粗,舌苔黄腻,脉弦滑;脑梗死、脑出血见上述证候者。
本品还有用于热毒内盛所致的肺性脑病、肝性脑病、胰腺炎的报道。
肌内注射,一日2~4ml。重症患者静脉滴注,一日20~40ml,以10%葡萄糖注射液200ml或氯化钠注射液100ml稀释后使用。
本品不良反应以各种类型过敏反应为主,其中严重过敏反应包括过敏性休克、急性喉头水肿、过敏性哮喘、过敏性间质性肾炎,并有死亡病例,不良反应以首用即发型和速发型为主。此外,还可发生剥脱性皮炎。
1.药物过敏史者慎用。如出现过敏反应应及时停药并做脱墩处理。
2.久病体虚患者慎用。
3.临床应用本品时,医护人员应在给药后30分钟内对患者进行严密监护,若出现皮肤瘙痒、心悸、胸闷、发绀等症状时应立即停药并给予积极治疗。
4.若发现浑浊、沉淀、变色、漏气或瓶身细微破裂,均不得使用。如经10%葡萄糖或氯化钠注射液稀释后,出现浑浊亦不得使用。
5.本品不能与硫酸庆大霉素、青霉素G钾、肾上腺素、阿拉明、乳糖酸红霉素、多巴胺、山梗菜碱、硫酸美芬丁胺配伍使用。
6.本品稀释以后,必须在4小时以内使用。
7.本品稀释后滴速,儿童以20~40滴/分为宜,成年人以40~60滴/分为宜。
(1)取本品10ml,置水浴上蒸干,放冷,残渣加乙醇1ml使溶解,取上清液作为供试品溶液。另取栀子苷对照品,加乙醇制成每1ml含4mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以乙酸乙酯-丙酮-甲酸-水(5:5:1:1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
(2) 取本品1ml,加乙醇2ml,混匀,作为供试品溶液。另取胆酸对照品、猪去氧胆酸对照品,加乙醇制成每1ml各含1mg的混合溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以异辛烷-乙酸乙酯-冰醋酸(15:7:5)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
(3)取黄芩苷对照品,加70%乙醇制成每1ml含1mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取〔鉴别〕(2)项下的供试品溶液及上述对照品溶液各2μl,分别点于同一聚酰胺薄膜上,以醋酸为展开剂,展开,取岀,晾干,喷以1%三氯化铁乙醇溶液。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
山银花 取本品20ml,加盐酸3滴,边加边搅拌,滤过,滤液加氢氧化钠试液调节pH值至7,用水饱和的正丁醇振摇提取2次,每次30ml,合并正丁醇液,用氨试液洗涤两次,每次30ml,分取正丁醇层,蒸干,残渣加甲醇2ml使溶解,作为供试品溶液。另取灰毡毛忍冬皂苷乙对照品,加甲醇制成每1ml含1mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各2μl,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇-水(6:4:1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,供试品色谱中,在与对照品色谱相应的位置上,不得显相同颜色的斑点。
溶液的颜色 精密量取本品1ml,置50ml量瓶中,加水稀释至刻度,摇匀,与黄色10号标准比色液(通则0901第一法)比较,应不得更深。
pH值 应为6.8~7.5(通则0631)。
炽灼残渣 精密量取本品5ml,依法测定(通则0841),每1ml应为3.0~8.5mg。
总固体 精密量取本品2ml,置105℃干燥至恒重的蒸发皿中,蒸干,在105℃干燥2小时,移至干燥器中,冷却30分钟,迅速精密称定重量,每1ml遗留残渣应为30~60mg。
有关物质 除蛋白质、树脂、草酸盐外,照注射剂有关物质检查法(通则2400)检查,应符合规定。
蛋白质 取本品1ml,加糅酸试液1~3滴,不得出现浑浊。
树脂 取本品5ml,加三氯甲烷10ml,振摇提取,分取三氯甲烷液,置水浴上蒸干,残渣加冰醋酸2ml使溶解,置具塞试管中,加水3ml,混匀,放置30分钟,可有轻微浑浊,不得出现絮状物或沉淀。
草酸盐 取本品5ml,置离心管中,滴加6mol/L盐酸溶液5滴,搅匀,离心,吸取上清液,滤过,取滤液2ml,调节pH值至5~6,加3%氯化钙溶液2~3滴,放置10分钟,不得出现沉淀。
重金属 精密量取本品1ml,置坩埚中,蒸干,再缓缓炽灼至完全灰化,放冷,照重金属检查法(通则0821第一法)检查,含重金属不得过10mg/kg。
异常毒性 取本品,依法检查(通则1141),静脉注射给药,剂量按每只小鼠注射0.5ml,应符合规定。
过敏反应 取本品,依法检查(通则1147),应符合规定。
热原 取本品,依法检查(通则1142),剂量按家兔体重每1kg注射5ml,应符合规定。
溶血与凝聚 取本品,依法检查(通则1148),应符合规定。
其他 应符合注射剂项下有关的各项规定(通则0102)。
照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂(色谱柱Phenomenex Luna C18 250mm×4.6mm,5μm);以乙腈为流动相A,以0.1%甲酸溶液为流动相B,按下表中的规定进行梯度洗脱;流速为0.5ml/min;检测波长为254nm;柱温为25℃。理论板数按栀子苷峰计算应不低于100000。

参照物溶液的制备 取栀子苷对照品适量,精密称定,加甲醇制成每1ml含0.2mg的溶液,即得。
供试品溶液的制备 取本品,滤过,取续滤液,即得。
测定法 分别精密吸取参照物溶液与供试品溶液各10μl,注入液相色谱仪,测定,记录65分钟内的色谱峰,即得。
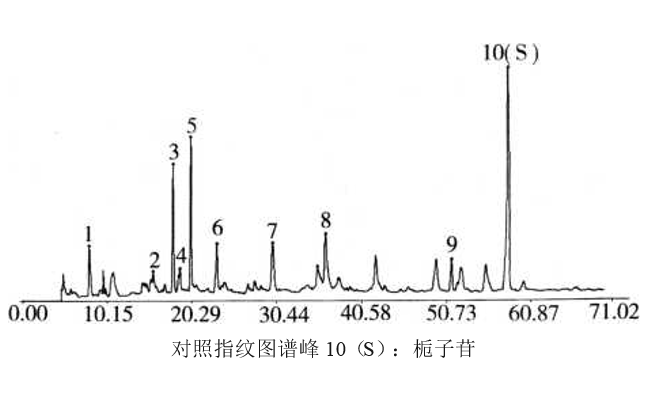
本品指纹图谱中应呈现与栀子苷对照品色谱峰保留时间一致的色谱峰,并应出现10个共有峰,以1、3、5、6、7、8、9、10(S)号峰为标记,经中药色谱指纹图谱相似度评价系统软件计算,与对照指纹图谱相比较,相似度不得低于0.80。
胆酸 猪去氧胆酸 照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以甲醇-乙腈-0.1%甲酸溶液(68:17:15)为流动相;用蒸发光散射检测器检测。理论板数按胆酸峰计算应不低于4000。
对照品溶液的制备 取胆酸对照品、猪去氧胆酸对照品适量,精密称定,加甲醇制成每1ml含胆酸0.2mg和猪去氧胆酸0.1mg的混合溶液,即得。
供试品溶液的制备 精密量取本品1ml,置10ml量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
测定法 分别精密吸取对照品溶液5μl、15μl,供试品溶液10μl,注入液相色谱仪,测定,以外标两点法对数方程计算,即得。
本品每1ml含胆酸(C24H40O5)应为1.50~3.25mg;含猪去氧胆酸(C24H40O4)应为1.00~3.20mg。
栀子 照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以乙腈-水(10:90)为流动相;检测波长为238nm。理论板数按栀子苷峰计算应不低于3000。
对照品溶液的制备 取栀子苷对照品适量,精密称定,加甲醇制成每1ml含30μg的溶液,即得。
供试品溶液的制备 精密量取本品5ml,置50ml量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
测定法 分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
本品每1ml含栀子以栀子苷(C17H24O10)计,不得少于0.10mg。
黄芩苷 照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸(47:53:0.2)为流动相;检测波长为276nm。理论板数按黄芩苷峰计算应不低于3000。
对照品溶液的制备 取黄芩苷对照品适量,精密称定,置100ml量瓶中,加70%乙醇适量使溶解,加流动相1ml,再加70%乙醇稀释至刻度,摇匀,精密量取5ml,置10ml量瓶中,加70%乙醇稀释至刻度,摇匀,即得(每1ml含黄芩苷50μg)。
供试品溶液的制备 精密量取本品1ml,置100ml量瓶中,加70%乙醇稀释至刻度,摇匀,滤过,取续滤液,即得。
测定法 分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
本品每1ml含黄芩苷(C21H18O11),应为3.5~5.5mg。
总氮量 精密量取本品0.5ml,照氮测定法(通则0704第二法)测定,即得。
本品每1ml含总氮(N)应为2.2~3.0mg。
(1)每支装2ml (2)每支装10ml
密闭。
[1]胆酸 取本品20mg,精密称定,置100ml量瓶中,加甲醇使溶解并稀释至刻度,摇匀,照清开灵注射液〔含量测定〕胆酸 猪去氧胆酸项下方法,依法测定。
本品含胆酸(C24H40O5)不得少于80.0%。
[2] 猪去氧胆酸 取本品10mg,精密称定,置100ml量瓶中,加甲醇使溶解并稀释至刻度,摇匀;照清开灵注射液〔含量测定〕胆酸 猪去氧胆酸项下方法,依法测定。
本品含猪去氧胆酸(C24H40O4)不得少于80.0%。
[3] 黄芩苷 取本品10mg,精密称定,置100ml量瓶中,加70%乙醇适量使溶解,加流动相1ml,再加70%乙醇稀释至刻度,摇匀;精密量取5ml,置10ml量瓶中,加70%乙醇稀释至刻度,摇匀,照清开灵注射液〔含量测定〕黄芩苷项下方法,依法测定。
本品含黄芩苷(C21H18O11)不得少于90.0%。
1、中华人民共和国药典:2020年版. 一部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1574-2
2、中华人民共和国药典临床用药须知:2015年版. 中药成方制剂卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9405-3
