登录/
注册
登录/
注册
培哚普利叔丁胺
PeiduopuliShuding’an
Perindopriltert-Butylamine
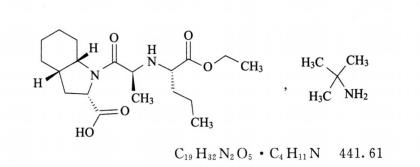
本品为(2S,3aS,7aS)-1-[(S)-N-[(S)-1-乙氧羰酰基丁基]丙氨酰]八氢-2-吲哚甲酸叔丁铵盐。按无水物和无溶剂物计算,含C19H32N2O5·C4H11N不得少于99.0%。
本品为白色或类白色结晶性粉末。
本品在水或乙醇中易溶。
比旋度取本品,精密称定,加乙醇溶解并定量稀释制成每1ml中约含10mg的溶液,依法测定(通则0621),比旋度应为—66°至—69°。
①高血压,可单独应用或与其他降压药如利尿药合用;②心力衰竭,可单独应用或与强心药利尿药同用。
口服成人(1)治疗高血压起始一次2mg,一日1次,以后按需要可递增至4mg,一日1次,最多为8mg,一日1次。常用维持量为4mg,一日4次。
(2)治疗心力衰竭一次2mg,一日1次,如证明对血压无不利影响,可加至4~8mg,一日1次。建议∶30ml/min<肌酐清除率<60ml/min时,一日2mg;15ml/min≤肌酐清除率<30ml/min时,隔日2mg。
(1)药效学 本品在体内水解为培哚普利拉,成为一种竞争性的血管紧张素转换酶抑制药。①降压,本品为竞争性血管紧张素转换酶抑制药,使血管紧张素Ⅰ不能转化为血管紧张素Ⅱ,结果血浆肾素活性增高,醛固酮分泌减少,血管阻力减低。本品还抑制缓激肽的降解;也可直接作用于周围血管而降低阻力,心排血量不变或增多,肾小球滤过率不变。卧位与立位降压作用无差别。②减低心脏负荷,心力衰竭时本品扩张动脉与静脉,降低周围血管阻力或后负荷,减低肺毛细血管嵌顿压或前负荷,也降低肺血管阻力,因而改善心排血量,运动耐量时间延长。
(2)药动学 口服本品后迅速吸收,吸收率为65%~70%,吸收后主要在肝内转化为有活性的培哚普利拉与无活性的葡萄糖醛酸盐,食物可使其转化减低。口服本品后3~4小时血中培哚普利拉浓度达高峰。口服剂量中的75%从尿中以原形与代谢产物排出,其余从粪中排出。10%~20%培哚普利拉与血浆蛋白结合。每日服用1次本品,平均达到稳定状态的时间是4日,作用累积半衰期为24小时。培哚普利拉的t1/2为9小时。肾功能衰竭时延长。本品和培哚普利拉可被透析清除。口服本品后1小时起作用,4~8小时达峰作用,作用维持约24小时。
(1)常见头痛、眩晕、疲乏、嗜睡、恶心、咳嗽。最常见的停药原因为头痛和咳嗽。
(2)少见症状性低血压、直立性低血压、晕厥、心悸、周围性水肿、皮疹、皮炎、便秘、胃炎、焦虑、失眠、感觉异常、关节痛、肌痛、哮喘等。
(3)罕见血管神经性水肿,如出现即应停药;如有粒细胞缺乏、骨髓抑制应停药。
(1)对本品或其他血管紧张素转换酶抑制药过敏者。
(2)孤立肾、移植肾、双侧肾动脉狭窄、严重肾功能减退者。
(3)妊娠、哺乳期妇女。
(4)美国FDA妊娠期药物安全性分级为口服给药C如在妊娠中、晚期用药D。
(1)在小儿中研究不充分,其安全性和疗效有待明确。
(2)对诊断的干扰用本品时可有∶①血尿素氮、肌酐浓度增高,常为暂时性,在有肾病或严重高血压而血压迅速下降时易出现;②偶有血清肝脏酶增高;③血钾轻度增高,尤其在有肾功能障碍者。
(3)下列情况慎用①自身免疫性疾病如严重系统性红斑狼疮,此时白细胞或粒细胞减少的机会增多;②骨髓抑制;③脑或冠状动脉供血不足,可因血压降低而缺血加重;④血钾过高;⑤肾功能障碍而致血钾高,白细胞及粒细胞减少,并使本品潴留;⑥严格饮食限制钠盐或进行透析治疗者,首剂应用本品可能发生突然而严重的低血压。
(4)用本品时发生血管神经性水肿时停用本品,皮下注射肾上腺素,静脉注射氢化可的松。
(5)用本品过量时,用扩容纠正低血压,必要时做透析治疗。
(6)用本品期间随访检查∶①对有肾功能障碍或有白细胞缺乏的患者最初3个月内每2周检查白细胞计数及分类计数1次,此后定期检查;②尿蛋白检查,每月1次。
(7)有报道,在采用高渗透膜进行透析时应用ACE抑制药的患者中,有发生迟发性危及生命的过敏样反应的病例。
(1)与利尿药同用降压作用增强,可能引起严重低血压,故原用利尿药者应停药或减量,本品开始用小剂量,逐渐调整剂量。
(2)与其他扩血管药同用可能致低血压,如需合用应从小剂量开始。
(3)与保钾利尿药如螺内酯、氨苯蝶啶、阿米洛利同用可能引起血钾过高。
(4)非甾体类抗炎镇痛药尤其吲哚美辛可通过抑制肾前列腺素合成,引起水、钠潴留,与本品同用时可使本品的降压作用减弱。
(5)与其他降压药同用时降压作用加强,其中与引起肾素释出或影响交感活性的药物呈较大的相加作用,与β受体拮抗药呈小于相加的作用。
培哚普利叔丁胺片:(1)2mg;(2)4mg;(3)8mg。
(1)照薄层色谱法(通则 0502)试验。
供试品溶液 取本品适量,加甲醇溶解并稀释制成每 1ml 中约含 20mg 的溶液。
对照品溶液 取培哚普利叔丁胺对照品适量,加甲醇溶解并稀释制成每 1ml 中约含 20mg 的溶液。
色谱条件 釆用硅胶 G 薄层板,以甲醇-甲苯-冰醋酸(60:40:1)为展开剂。
测定法 吸取供试品溶液与对照品溶液各 10μl,分别点于同一薄层板上,展开,晾干,置饱和碘蒸气中显色 20 小时以上。
结果判定 供试品溶液所显两个主斑点的位置和颜色应与对照品溶液相同。
(2)取本品和培哚普利叔丁胺对照品各适量,分别加流动相 A 使溶解并稀释制成每 1ml 中约含 0.3mg 的溶液,作为供试品溶液和对照品溶液。照有关物质项下的方法,取供试品溶液和对照品溶液各 20μl,分别注入液相色谱仪,记录色谱图。供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集 1204 图)一致。
以上(1)、(2)两项可选做一项。
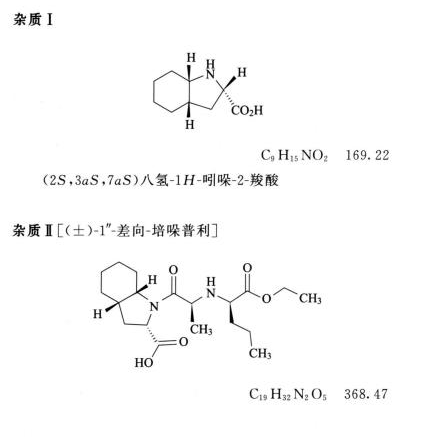
(2S,3aS,7aS)八氢-1H-吲哚-2-羟酸(杂质 I)照薄层色谱法(通则 0502)试验。
供试品溶液 取本品,精密称定,加甲醇溶解并定量稀释制成每 1ml 中约含 20mg 的溶液。
对照品贮备液 取杂质 I 对照品适量,精密称定,加甲醇溶解并定量稀释制成每 1ml 中约含 0.2mg 的溶液。
对照品溶液 精密量取对照品贮备液适量,用甲醇定量稀释制成每 1ml 中约含 50μg 的溶液。
系统适用性溶液 取对照品贮备液适量,与 2%叔丁胺的甲醇溶液等体积混合。
色谱条件 采用硅胶 G 薄层板,以甲醇-甲苯-冰醋酸(60:40:1)为展开剂。
测定法 吸取供试品溶液、对照品溶液与系统适用性溶液各 10μl,分别点于同一薄层板上,展开,晾干,以饱和碘蒸气显色 20 小时以上。
系统适用性要求 系统适用性溶液应显两个完全分离的清晰斑点。
限度 供试品溶液如显与杂质 I 相同的斑点,与对照品溶液的主斑点比较,不得更深(0.25%)。
立体异构体 照高效液相色谱法(通则 0512)测定。
供试品溶液 取本品,精密称定,加乙醇溶解并稀释制成每 1ml 中约含 2mg 的溶液。
对照溶液 精密量取供试品溶液 1ml,置 100ml 量瓶中,用乙醇稀释至刻度,摇匀,精密量取 1ml,置 10ml 量瓶中,用乙醇稀释至刻度,摇匀。
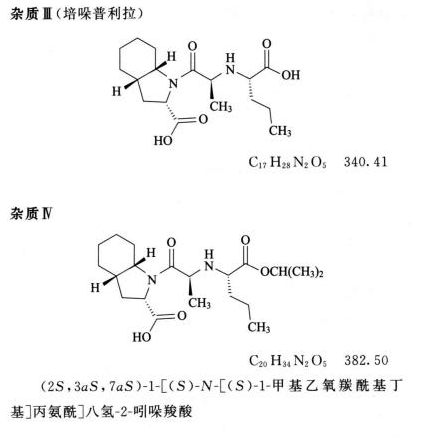
系统适用性溶液 取含有培哚普利叔丁胺和杂质 Ⅱ 的混合对照品(杂质 Ⅱ 含量不低于 0.1%)适量,加乙醇溶解并稀释制成每 1ml 中约含 2mg 的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(IntersilODS-3 C18 柱,4.6mm X 250mm,5μm或效能相当的色谱柱);以 0.15%庚烷磺酸钠溶液(用 35%高氯酸溶液调节 pH 值至 2.0)-乙腈-正戊醇(780:217:3)为流动相;检测波长为 215nm,柱温为 50℃;进样体积 10μl。
系统适用性要求 系统适用性溶液色谱图中,培哚普利峰的保留时间约为 100 分钟,杂质 Ⅱ 峰的峰高与杂质 Ⅱ 峰和主成分峰之间的峰谷比应大于 3。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的 1.5 倍。
限度 供试品溶液色谱中,杂质 Ⅱ 峰和相对保留时间在 0.6~1.4 之间的各单个杂质峰面积均不得大于对照溶液的主峰面积(0.1%)。
有关物质 照高效液相色谱法(通则 0512)测定。溶液均应置于 4℃以下保存。
供试品溶液 取本品,加流动相 A 溶解并稀释制成每 1ml 中约含 3mg 的溶液。
对照溶液 精密量取供试品溶液 1ml,置 100ml 量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液 取培哚普利叔丁胺与杂质 Ⅲ 对照品各适量,加流动相溶解并稀释制成每 1ml 中各约含 0.2mg 的混合溶液。
灵敏度溶液 精密量取对照溶液 1ml,置 50ml 量瓶中,用流动相稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(ZorbaxSB-C18 柱,4.6mm X 250mm,5μm或效能相当的色谱柱);以甲醇-磷酸盐缓冲溶液(取磷酸二氢钾 2g,加水使溶解,再加磷酸 3ml 和三乙胺 3ml,用水稀释至 1000ml)(48:52)为流动相 A,以甲醇-水(75:25)为流动相 B。按下表进行梯度洗脱,检测波长为 215nm;柱温为 50℃;进样体积 20μl。
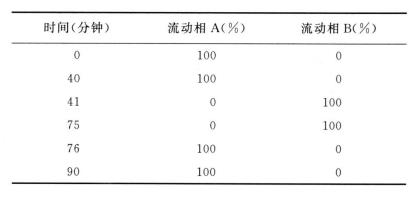
系统适用性要求 系统适用性溶液色谱图中,培哚普利峰的保留时间约为 12 分钟,培哚普利峰与杂质 Ⅲ 峰之间的分离度应大于 6.0。灵敏度溶液色谱图中,主成分色谱峰的信噪比应不小于 10。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中除叔丁胺峰外,如有与杂质 Ⅲ 峰保留时间一致的色谱峰,其峰面积不得大于对照溶液主峰面积的 0.3 倍(0.3%);如有相对保留时间为 1.77~1.90 的杂质 Ⅳ 峰,其峰面积不得大于对照溶液主峰面积的 0.4 倍(0.4%);其他单个杂质峰面积不得大于对照溶液主峰面积的 0.2 倍(0.2%),各杂质峰面积的和不得大于对照溶液的主峰面积(1.0%),小于灵敏度溶液主峰面积 2.5 倍的色谱峰忽略不计。
残留溶剂 照残留溶剂测定法(通则 0861 第二法)测定。
供试品溶液 取本品 0.5g,精密称定,置顶空瓶中,精密加水 5ml 使溶解,密封。
对照品溶液 分别取丙酮 500mg、二氯甲烷 60mg、乙酸乙酯 500mg 和四氢呋喃 72mg,精密称定,置 100ml 量瓶中,用水稀释至刻度,摇匀,精密量取 5ml,置 50ml 量瓶中,用水稀释至刻度,摇匀,精密量取 5ml,置顶空瓶中,密封。
色谱条件 以 6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液的毛细管柱为色谱柱(0.32mm X 30m,1.8μm);程序升温;初始温度为 40℃,维持 18 分钟,以每分钟 20℃的速率升温至 120℃,维持 5 分钟;进样口温度为 200℃;检测器温度为 250℃;顶空瓶平衡温度为 80℃,平衡时间为 30 分钟。
系统适用性要求 对照品溶液色谱图中,各成分峰间的分离度均应符合要求。
测定法 精密量取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度 按外标法以峰面积计算,丙酮、二氯甲烷、乙酸乙酯和四氢呋喃的残留量均应符合规定。
水分 取本品,照水分测定法(通则 0832 第一法 1)测定,含水分不得过 1.0%。
炽灼残渣 取本品 1.0g,依法检查(通则 0841),遗留残渣不得过 0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则 0821 第二法),含重金属不得过百万分之十。
取本品约 0.16g,精密称定,加冰醋酸 50ml 使溶解,照电位滴定法(通则 0701),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每 1ml 高氯酸滴定液(0.1mol/L)相当于 22.08mg 的C19H32N2O5 · C4H11N。
抗高血压药。
30℃以下密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
