登录/
注册
登录/
注册
吸附无细胞百白破联合疫苗
XifuWuxibaoBaiBaiPoLianheYimiao
Diphtheria,TetanusandAcellularPertussisCombinedVaccine,Adsorbed
本品系由无细胞百日咳疫苗原液、白喉类毒素原液及破伤风类毒素原液加入氢氧化铝佐剂制成。用于预防百日咳、白喉、破伤风。
生产和检定用设施、原材料及辅料、水、器具、动物等应符合“凡例”的有关要求。
2.1 混合前单价原液
2.1.1 无细胞百日咳疫苗原液制造应符合本品种附录的规定。
2.1.2 白喉类毒素原液制造应符合“吸附白喉疫苗”中2.1~2.2项的规定。
2.1.3 破伤风类毒素原液制造应符合“吸附破伤风疫苗”中2.1~2.2项的规定。
2.1.4 原液检定
2.1.4.1 百日咳疫苗原液检定
按本品种附录中2项进行。
2.1.4.2 白喉类毒素原液检定
按“吸附白喉疫苗”中3.1项进行。
2.1.4.3 破伤风类毒素原液检定
按“吸附破伤风疫苗”中3.1项进行。
2.2 半成品
2.2.1 佐剂配制
佐剂的制备和检定(通则3650)应符合批准的要求。
2.2.2 合并及稀释
将白喉类毒素、破伤风类毒素及无细胞百日咳疫苗原液加入已稀释的佐剂内,调pH值至5.8~7.2,使每1ml半成品含无细胞百日咳疫苗原液应不高于18μgPN;白喉类毒素应不高于25Lf;破伤风类毒素应不高于7Lf。
2.2.3 半成品检定
按3.1项进行。
2.3 成品
2.3.1 分批
应符合“生物制品分包装及贮运管理”规定。
2.3.2 分装
应符合“生物制品分包装及贮运管理”规定。
2.3.3 规格
每瓶0.5ml、1.0ml、2.0ml、5.0ml。每1次人用剂量0.5ml,含无细胞百日咳疫苗效价应不低于4.0IU,白喉疫苗效价应不低于30IU,破伤风疫苗效价应不低于40IU。
2.3.4 包装
应符合“生物制品分包装及贮运管理”规定。
3.1 半成品检定
3.1.1 无菌试验
依法检查(通则1101),应符合规定。
3.1.2 吸附率检查
将供试品离心取上清液,同时取供试品进行适当稀释,选取0~100μg/ml范围作为对照品溶液浓度,依法测定[通则0731第二法福林酚法(Lowry法)方法2]供试品及其上清液的蛋白含量,再按下式计算吸附率,应不低于95%。
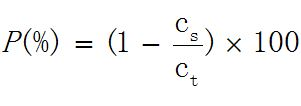
式中 P为吸附率,%;
cs为供试品上清液的蛋白含量,μg/ml;
ct为供试品的蛋白含量,μg/ml。
3.2 成品检定
3.2.1 鉴别试验
3.2.1.1 无细胞百日咳疫苗
可选择下列一种方法进行:(1)疫苗注射动物应产生抗体(按3.2.4.1项进行);(2)采用酶联免疫吸附法检测PT、FHA抗原,应含有相应抗原(通则3417);(3)其他适宜的抗原抗体反应试验。
3.2.1.2 白喉类毒素
可选择下列一种方法进行:(1)疫苗注射动物应产生抗体(通则3505);(2)疫苗加枸椽酸钠或碳酸钠将佐剂溶解后,做絮状试验(通则3506),应岀现絮状反应;(3)疫苗经解聚液溶解佐剂后取上清液,做凝胶免疫沉淀试验(通则3403),应出现免疫沉淀反应。
3.2.1.3 破伤风类毒素
可选择下列一种方法进行:(1)疫苗注射动物后应产生破伤风抗体(通则3504);(2)疫苗加入枸椽酸钠或碳酸钠将吸附剂溶解后做絮状试验(通则3506),应出现絮状反应;(3)疫苗经解聚液溶解佐剂后取上清液,做凝胶免疫沉淀试验(通则3403),出现免疫沉淀反应。
3.2.2 物理检查
3.2.2.1 外观
振摇后应呈均匀乳白色混悬液,无摇不散的凝块或异物。
3.2.2.2 装量
依法检查(通则0102),应不低于标示量。
3.2.2.3 渗透压摩尔浓度
依法测定(通则0632),应符合批准的要求。
3.2.3 化学检定
3.2.3.1 pH值
应为5.8~7.2(通则0631)。
3.2.3.2 铝含量
应为0.17~0.26mg/剂(通则3106)。
3.2.3.3 硫柳汞含量
应不高于0.05mg/剂(通则3115)。
3.2.3.4 游离甲醛含量
应不高于0.1mg/剂(通则3207第一法)。
3.2.3.5 戊二醛含量
应小于0.005mg/剂(通则3204)。
3.2.4 效价测定
3.2.4.1 无细胞百日咳疫苗
按“吸附百白破联合疫苗”中附录2进行。以适宜的稀释倍数稀释至第一个免疫剂量,再按5倍系列稀释。免疫时间为21天。每1次人用剂量的免疫效价应不低于4.0IU,且95%可信限的低限应不低于2.0IU。如达不到上述要求时可进行复试,但所有的有效试验结果必须以几何平均值(如用概率分析法时,应用加权几何平均)来计算。达到上述要求即判为合格。
3.2.4.2 白喉疫苗
每1次人用剂量中白喉类毒素的免疫效价应不低于30IU(通则3505)。
3.2.4.3 破伤风疫苗
每1次人用剂量中破伤风类毒素的免疫效价应不低于40IU(通则3504)。
3.2.5 无菌检查
依法检查(通则1101),应符合规定。
3.2.6 特异性毒性检查
3.2.6.1 无细胞百日咳疫苗
按本品种附录中2.5项进行。
3.2.6.2 白喉、破伤风疫苗
用体重250~350g豚鼠,每批制品不少于4只,每只腹部皮下注射2.5ml,分两侧注射,每侧1.25ml,观察30天。注射部位可有浸润,经5~10天变成硬结,可能30天不完全吸收。在第10天、第20天、第30天称体重,到期体重比注射前增加,局部无化脓、无坏死、无破伤风症状及无晚期麻痹症者为合格。
3.2.7 毒性逆转试验
每批供试品置37℃ 4周,按本品种附录中2.6项进行。
3.2.8 细菌内毒素检查
每1次人用剂量应不高于100EU(通则1143)。
于2~8℃避光保存和运输。自生产之日起,有效期为24个月;自百日咳原液脱毒之日起,疫苗总有效期不得超过36个月。
无细胞百日咳疫苗原液制造及检定要求。
应符合“生物制品分包装及贮运管理”规定和批准的内容。
附录 无细胞百日咳疫苗原液制造及检定要求
本品系由百日咳杆菌的培养物或其上清液,经硫酸铵盐析和蔗糖密度梯度离心法提取百日咳毒素(PT)和丝状血凝素(FHA)等有效组分,经脱毒制成。用于制备吸附无细胞百白破联合疫苗。
1 制造
1.1 菌种
生产用菌种应符合“生物制品生产检定用菌毒种管理及质量控制”的有关规定。
1.1.1 名称及来源
生产用菌种应采用百日咳I相CMCC 58003(CS株)或其他适宜菌株。
1.1.2 种子批的建立
应符合“生物制品生产检定用菌毒种管理及质量控制”的规定。
1.1.3 种子批的传代
工作种子批菌种启开后传代不应超过10代用于生产。
1.1.4 种子批的检定
1.1.4.1 培养特性
于包-姜(Bordet-Gengou)培养基或其他适宜培养基上培养,各菌株应具有典型的形态,葡萄糖、尿素酶、硝酸盐、枸椽酸盐、半固体(动力)营养琼脂结果均应为阴性。
1.1.4.2 血清学试验
取经35~37℃培养40~48小时的菌苔,混悬于0.85%~0.90%氯化钠溶液或PBS内,制成适宜浓度的菌悬液,与I相参考血清做定量凝集反应,凝集效价应达到血清原效价之半。并同时进行Fim2、Fim3的血清学检测,应为阳性。
1.1.4.3 皮肤坏死试验
取经35~37℃培养40~48小时的菌苔,混悬于PBS内,并稀释成不同浓度的菌液;取家兔或豚鼠至少2只,分别用每一稀释度的菌液皮内注射0.1ml,经72小时观察注射部位的皮肤反应,其中至少1只家兔或豚鼠在注射含菌4.0×107以下稀释度的部位出现出血性坏死者,为阳性反应,判为合格。
1.1.4.4 毒力试验
用体重16~18g的小鼠至少3组,每组至少10只,在麻醉状态下从鼻腔滴入经培养20~24小时、以PBS稀释的菌液0.05ml,观察14天,记录小鼠生死情况,按Reed-Muench法计算LD50,1LD50的菌数应不高于1.2×108。
1.1.4.5 效价测定
按“吸附百白破联合疫苗”附录2进行。
1.1.5 菌种保存
种子批应冻干保存于8℃及以下。
1.2 原液
1.2.1 生产用种子
将工作种子批菌种启开后,接种于改良包-姜培养基或活性炭半综合培养基或其他适宜培养基上,于35~37℃培养不超过72小时,以后各代不超过48小时。传代菌种保存不得超过14天,工作种子批启开后用于生产时不应超过10代。
1.2.2 生产用培养基
应选用S-S(Stainer-Scholte)培养基或其他适宜培养基。
1.2.3 培养
可采用静置培养法或发酵罐培养法,培养过程应取样做纯菌检查。
1.2.4 收获和杀菌
培养物于对数生长期后期或静止期前期收获。在培养物中加入硫柳汞杀菌。
1.2.5 纯化
采用硫酸铵盐析和蔗糖密度梯度离心,收集PT、FHA有效组分。
1.2.6 蛋白氮含量测定
依法测定(通则0731第二法)。
1.2.7 纯度测定
采用聚丙烯酰胺凝胶电泳法或SDS-聚丙烯酰胺凝胶电泳法检测,应显示主要含有PT和FHA两种组分,且批间比例应保持一致。PT和FHA等有效组分应不低于总蛋白质含量的85%。
1.2.8 脱毒和匀化
采用甲醛溶液或戊二醛溶液脱毒,然后用适宜方法除去脱毒剂,再经超声波匀化处理即为原液。
2 检定
2.1 染色镜检
取供试品的沉淀物,涂片染色镜检,不应有百日咳杆菌和其他细菌。
2.2 效价测定
按“吸附百白破联合疫苗”附录2进行。即先将原液稀释至成品的浓度后,以适宜的稀释倍数为第一个免疫剂量,再按5倍系列稀释,免疫21天后攻击。
2.3 无菌检查
依法检查(通则1101),应符合规定。
2.4 不耐热毒素试验
用0.85%~0.90%氯化钠溶液将供试品稀释至半成品浓度的2倍,用48~72小时龄的乳鼠至少4只,每只皮内注射0.025ml,或用体重2.5kg的家兔至少2只,每只皮内注射0.1ml,观察4日,受试动物不得出现不耐热毒素引起的任何局部反应。
2.5 特异性毒性检查
毒性参考品按照每批标示进行稀释,将供试品稀释至与成品相同浓度。用体重14~16g NIH小鼠(雌性或雌雄各半),毒性参考品的每一稀释度和供试品各用一组,每组至少10只。每只小鼠腹腔注射0.5ml,分别进行2.5.1~2.5.3项试验。
2.5.1 小鼠白细胞增多试验
于注射后3天分别取小鼠末梢血进行白细胞计数。试验结果经统计学方法处理后,注射供试品的小鼠白细胞增多毒性的活性应不高于0.5LPU/ml。
2.5.2 小鼠组胺致敏试验
于注射后4天,每只小鼠腹腔注射0.5ml溶液(含二盐酸组胺4mg或二磷酸组胺2mg),30分钟后分别测小鼠肛温。试验结果经统计学方法处理后,供试品的小鼠组胺致敏毒性的活性应不高于0.8HSU/ml,且无动物死亡。
2.6 毒性逆转试验
每批供试品置37℃ 4周,然后按2.5.2项进行试验。
2.7 热原检查
用0.85%~0.90%氯化钠溶液将供试品稀释成半成品浓度的1/50,依法检查(通则1142),注射剂量按家兔体重每1kg注射1ml,应符合规定。
3 保存、运输及有效期
于2~8℃避光保存和运输。自原液脱毒之日起,疫苗总有效期为36个月。
中华人民共和国药典:2020年版.三部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1575-9
