登录/
注册
登录/
注册
复方盐酸阿米洛利片
Fufang Yansuan Amiluoli Pian
Compound Amiloride Hydrochloride Tablets
本品含盐酸阿米洛利(按C6H8ClN7O·HCl计)与氢氯噻嗪(C7H8ClNO4S2)均应为标示量的90.0%~110.0%。
盐酸阿米洛利 2.5g
氢氯噻嗪 25g
制成 1000片
本品为类白色至微黄色片。
水肿性疾病及难治性低钾血症的辅助治疗(由于螺内酯和氨苯蝶啶大部分需经肝脏代谢后排出体外,肝功能严重损害时,两药代谢减少,药物剂量不易控制,此时宜应用阿米洛利,因后者不需经肝脏代谢)。
口服 成人 开始一次2.5~5mg,一日1次,以后酌情调整剂量。一日最大剂量为20 mg。
(1)药效学 利尿作用于口服后2小时出现,6~10小时达高峰,可持续24小时。主要抑制末端远曲小管和集合管的Na+-K+和Na+-H+交换,从而Na+和水排出增多,而K+和H+排出减少。本药还使Ca2+和Mg2+排泄减少。本药与排钾利尿药合用,可明显减少钾的排泄,并部分减少Ca2+和Mg2+的排泄。而排Na+和水的作用则增强。其作用不依赖于醛固酮。
本药的促尿钠排泄和降压活性较弱,但与噻嗪类或袢利尿药合用有协同作用。本药 40 mg 与氨苯蝶啶200 mg的利尿作用相当,为目前潴钾利尿药中作用最强者。
(2)药动学 口服吸收不完全,生物利用度约为50%,食物可降低生物利用度。血浆蛋白结合率低,在体内不被代谢,t1/2为6~9小时。20%~50%经肾脏排泄,40%左右随粪便排出。
单独使用时高钾血症较常见。本药可引起高钾血症、低钠血症、高钙血症、轻度代谢性酸中毒;胃肠道反应如恶心、呕吐、食欲缺乏、腹痛、腹泻或便秘,头痛、头晕、直立性低血压、性功能下降;过敏反应表现为皮疹,甚至呼吸困难。
严重的反应有中性粒细胞减少(罕见)、再生障碍性贫血。
(1)对本药过敏者。
(2)肾功能减退(Cr>1.5mg/100 ml或BUN>30 mg/100 ml)者。
(3)高钾血症患者。
(4)留钾治疗(使用留钾药或补充钾)者。
(1)可引起高钾血症,如不纠正则可致死。高血钾常在与排钾利尿药合用时发生。肾功能损害、糖尿病患者发生率较高。应仔细监测每一名使用本药的患者。
(2)尚无实验证实本药能否经乳汁分泌。有证据显示该药可改变乳汁的分泌与组成,如果不能改用他药,应监测乳儿的不良反应以及是否摄入足够的乳汁。
(3)老年人应用本药较易出现高钾血症和肾功能损害等,用药期间应密切观察。
(4)对诊断的干扰 可使下列测定值升高:血糖(尤其是糖尿病患者),血肌酐和尿素氮(尤其是老年人和已有肾功能损害者),血钾、血镁及血浆肾素浓度。血钠浓度下降。
(5)下列情况慎用 ①无尿;②肾功能损害;③糖尿病;④糖尿病肾病;⑤电解质失衡和BUN增加;⑥代谢性或呼吸性酸中毒和低钠血症。
(6)美国FDA妊娠期用药安全性分级:口服给药B;D(如用于妊娠高血压)。
(1)与含碘造影剂合用,可增加发生急性肾功能衰竭的风险,给予造影剂之前应注意补足水分。
(2)与抗精神病药物合用,可增加发生直立性低血压的风险。
(3)与他克莫司合用,可发生致死性高血钾,肾功能不全者风险更大。
(4)与依普利酮或氨苯蝶呤等其他留钾利尿药合用,留钾的作用相加,引起高钾血症的风险增加,属禁忌。
复方盐酸阿米洛利片:每片含盐酸阿米洛利2.5mg 和氢氯噻嗪 25 mg。
在含量测定项下记录的色谱图中,供试品溶液两主峰的保留时间应与对照品溶液中相应两主峰的保留时间一致。
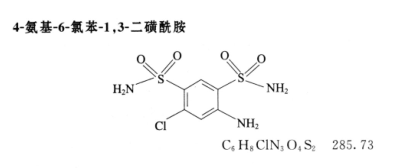
4-氨基-6-氯苯-1,3-二磺酰胺 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品10片,精密称定,研细,精密称取适量[约相当于盐酸阿米洛利(按C6H8ClN7O·HCl计)5mg],置50ml量瓶中,加甲醇15ml与0.1mol/L盐酸溶液2ml,超声使盐酸阿米洛利与氢氯噻嗪溶解,放冷,用水稀释至刻度,摇匀,滤过,取续滤液。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液 取4-氨基-6-氯苯-1,3-二磺酰胺、氢氯噻嗪对照品与盐酸阿米洛利对照品,加流动相溶解并稀释制成每1ml中各含0.1mg的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取磷酸二氢钾13.6g,加水80ml溶解后,用磷酸调节pH值至3.0,用水稀释至100ml)-甲醇-水(4:25:71)为流动相;检测波长为265nm;进样体积20µl。
系统适用性要求 系统适用性溶液色谱图中,理论板数按氢氯噻嗪峰计算不低于1500,4-氨基-6-氯苯-1,3-二磺酰胺峰、氢氯嚷嗪峰与阿米洛利峰之间的分离度均应符合要求。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有与系统适用性溶液中4-氨基-6-氯苯3-二磺酰胺峰保留时间一致的峰,其峰面积不得大于对照溶液中氢氯噻嗪峰面积(1.0%)。
含量均匀度 取本品1片,置25ml量瓶中,加甲醇7.5ml与0.1mol/L盐酸溶液1ml,照含量测定项下的方法,自“超声使盐酸阿米洛利与氢氯噻嗪溶解”起,依法测定,应符合规定(通则0941)。
溶出度 照溶出度与释放度测定法(通则0931第一法)测定。
溶出条件 以0.1mol/L盐酸溶液900ml为溶出介质,转速为每分钟100转,依法操作,经30分钟时,取溶出液20ml,滤过,取续滤液备用。
盐酸阿米洛利 供试品溶液取上述续滤液。
对照品溶液 取盐酸阿米洛利对照品,精密称定,加0.1mol/L盐酸溶液溶解并定量稀释制成每1ml中约含2.5µg的溶液。
测定法 取供试品溶液与对照品溶液,照紫外-可见分光光度法(通则0401),在365nm波长处分别测定吸光度,计算每片的溶出量。
限度 标示量的80%,应符合规定。
氢氯噻嗪供试品溶液 精密量取上述续滤液5ml,置50ml量瓶中,用0.1mol/L盐酸溶液稀释至刻度,摇匀。
对照品溶液 取氢氯噻嗪对照品,精密称定,加0.1mol/L盐酸溶液溶解并定量稀释制成每1ml中约含2.5µg的溶液。
测定法 取供试品溶液与对照品溶液,照紫外-可见分光光度法(通则0401),在272nm波长处分别测定吸光度,计算每片的溶出量。
限度 标示量的80%,应符合规定。
其他 应符合片剂项下有关的各项规定(通则0101)。
照高效液相色谱法(通则0512)测定。
供试品溶液 见4-氨基-6-氯苯-1,3-二磺酰胺项下。
对照品溶液 取氢氯噻嗪对照品约0.1g,精密称定,置100ml量瓶中,加甲醇20ml使溶解,精密加盐酸阿米洛利对照品溶液(取盐酸阿米洛利对照品,精密称定,加甲醇溶解并定量稀释制成每1ml中约含lmg的溶液)10ml,加0.1mol/L盐酸溶液4ml,用水稀释至刻度,摇匀。
色谱条件 见4-氨基-6-氯苯-1,3-二磺酰胺项下。检测波长为286nm;进样体积10µl。
系统适用性要求 理论板数按阿米洛利峰计算不低于1000,阿米洛利峰与氢氯噻嗪峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
利尿药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
